Seqirus: Zelllinie statt Hühnerei
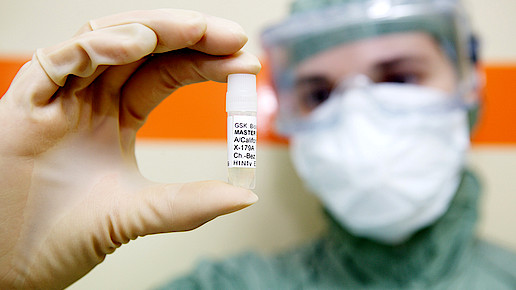
Grippeimpfstoff ohne Hühnereiweiß: Seqirus hat im Februar bei der Europäischen Arzneimittelagentur (EMA) die Zulassung für den ersten zellbasierten quadrivalenten Grippeimpfstoff (QIVc) beantragt.
Ab der Grippesaison 2019/2020 soll es so weit sein, dann soll QIVc gegen die saisonale Grippe auch in Europa zur Verfügung stehen. Die zellbasierte Vakzine soll vorerst ab einem Alter von vier Jahren zugelassen werden. Geplant ist jedoch eine Senkung der Altersgrenze auf sechs Monate – entsprechende klinische Studien wurden bereits gestartet.
Seqirus hat bereits 2016 für den QIVc Flucelvax von der US-Arzneimittelbehörde FDA eine Zulassung erhalten. Die Vakzine wird in North Carolina produziert. Eine Kapazitätsausweitung soll es ermöglichen, dort auch die für den europäischen Markt benötigten Impfdosen zu produzieren.
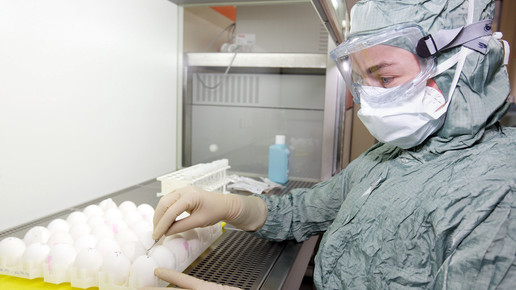
Bei der Herstellung der konventionellen Impfstoffe werden Hühnereier als Brutstätte verwendet. Einige Grippeviren können sich jedoch verändern, wenn sie eibasiert produziert und vermehrt werden; dieser Vorgang könnte die Wirksamkeit beeinflussen. Werden die Virusantigene auf Zellkulturen gezüchtet, sind sie laut Seqirus dem ursprünglich selektierten Virus ähnlicher. Somit könnte deren Wirksamkeit erweitert sein.
Außerdem könnten Personen mit klinisch sehr schwerer Hühnereiweißallergie profitieren. Die Betroffenen können bereits beim Zuführen geringster Mengen Hühnereiweiß eine Schockreaktion und Atemnot erleiden. Auch ein chronisches, therapiebedürftiges Asthma aufgrund einer Hühnereinweißallergie kann möglich sein. Diese Patienten sollen laut Paul-Ehrlich-Institut (PEI) nur unter besonderen Schutzmaßnahmen und anschließender Beobachtung geimpft werden.
Professor Dr. Markus Rose, Impfexperte, Allergologe und Kinderlungenarzt am Klinikum St. Georg in Leipzig, unterstützt diesen Ansatz: „Ein zellbasierter Vierfachgrippeimpfstoff erscheint nicht nur hochwirksam, sondern löst als Zusatzeffekt das in der Praxis bekannte Problem der Immunisierung von Hühnerei-Allergikern.“
Seqirus hatte mit Optaflu eine in einer Zelllinie gezüchtete trivalente Vakzine von Novartis übernommen. Verfügbar ist der Impfstoff jedoch nicht und andere Alternativen gibt es nicht. Optaflu hatte bereits 2007 die EU-Zulassung erhalten.







































APOTHEKE ADHOC Debatte