Sartane: EMA nimmt Hersteller in die Pflicht
Nach dem Valsartan-Skandal im Sommer 2018 fordert die Europäische Arzneimittelagentur (EMA) die Hersteller von Sartan-haltigen Arzneimitteln auf, ihre Herstellungsprozesse zu überprüfen und so weitere Nitrosamin-Verunreinigungen auszuschließen.
Den Unternehmen wird eine Übergangszeit von zwei Jahren gewährt. In diesem Zeitintervall sollen die Hersteller alle erforderlichen Änderungen vornehmen, die die Einhaltung der vorübergehend geltenden strikten Grenzwerte für Nitrosamine gewährleisten. Zum Ende der Übergangsfrist müssen die Unternehmen nachweisen, dass die produzierten Arzneimittel keine quantifizierbaren Mengen der Verunreinigungen enthalten. Dies ist Voraussetzung für das Inverkehrbringen der Angiotensin-II-Rezeptorblocker innerhalb der EU.
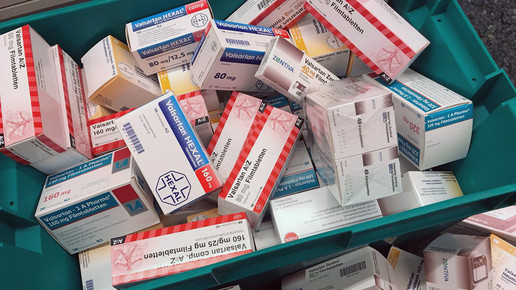
Grund für die Vorgabe ist die Rückrufwelle Sartan-haltiger Arzneimittel im Sommer 2018, die bis heute andauert. Valsartan musste aufgrund von Verunreinigungen mit dem Nitrosamin N-Nitrosodimethylamin (NDMA) und N-Nitrosodiethylamin (NDEA) zurück. Zum Teil waren die aktiven Substanzen mit einem, zum Teil mit beiden als potentiell für den Menschen kanzerogen eingestuften Substanzen verunreinigt. Rückrufe aufgrund der Anwesenheit von NDEA gab es auch bei Irbesartan und Losartan.
Im August gab die EMA eine erste Einschätzung zum potentiellen Patientenrisiko für NDMA ab. Anhand der Konzentration schätzte die EMA dass es bei 5000 Patienten, die über einen Zeittraum von sieben Jahren täglich mit der höchsten Valsartan-Dosis von 320 mg behandelt werden, einen zusätzlichen Krebsfall geben könne. Dennoch sei es „wichtig zu beachten, dass es kein unmittelbares Risiko für die Patienten gibt“. Jetzt liegen neue Zahlen vor. Die EMA schätzt, das bei 100.000 Patienten, die mit Valsartan des chinesischen Lohnherstellers Zhejiang Huahai Pharmaceuticals in der höchsten Dosierung über einen Zeitraum von sechs Jahren täglich behandelt wurden, 22 zusätzliche Krebsfälle aufgrund der Anwesenheit von NDMA auftreten. NDEA kann schätzungsweise zu acht zusätzlichen Krebsfällen bei 100.00 Patienten führen, die in der höchsten Dosis über einen Zeitraum von vier Jahren täglich behandelt wurden.
Die Verunreinigungen waren bei Routineuntersuchungen nicht festgestellt worden, sondern erst als im Sommer die Bombe platzte und aufgrund der Meldung eines spanischen Herstellers die Anwesenheit der Nitrosamine in der aktiven Substanz des chinesischen Lohnherstellers entdeckt wurde. Die Nitrosamine können während des Herstellungsprozesses unter bestimmten Bedingungen – wie bestimmten Lösungsmitteln oder Reagenzien bei der Bildung des Tetrazolringes – entstehen. Oder wenn die Hersteller kontaminierte Reagenzien oder Geräte im Herstellungsprozess verwenden.
Während der Übergangszeit werde das Ziel verfolgt, keine quantifizierbaren Nitrosamin-Verunreinigungen in den Sartanen nachzuweisen. Für NDMA und NDEA gelten internationale Grenzwerte. Präparate, die außerhalb dieser Grenzwerte liegen, dürfen nicht mehr innerhalb der EU in den Verkehr gebracht werden. Die Grenzwerte basieren auf der maximalen täglichen Aufnahme, die aus Tierversuchen abgeleitet wurde. Für NDMA sind es 96 Nanogramm und für NDEA 26,5 Nanogramm. Dividiert diese Werte durch die tägliche zulässige Maximaldosis der einzelnen Wirkstoffe, ergibt sich der zulässige Grenzwert in parts per million (ppm).
- Candesartan 32 mg: Limit ppm NDMA 3,000 und NDEA 0,820
- Irbesartan 300 mg: Limit ppm NDMA 0,320 und NDEA 0,088
- Losartan 150 mg: Limit ppm NDMA 0,640 und NDEA 0,177
- Olmesartan 40 mg: Limit ppm NDMA 2,400 und NDEA 0,663
- Valsartan 320 mg: Limit ppm NDMA 0,300 und NDEA 0,082.























APOTHEKE ADHOC Debatte