Microvionin: Neues MRSA-Antibiotikum entdeckt
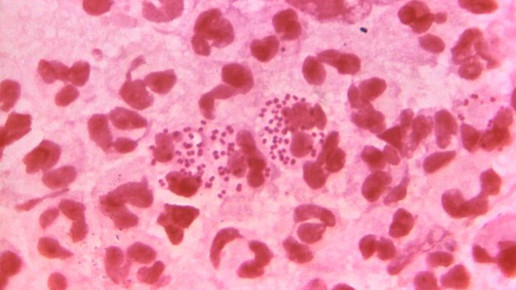
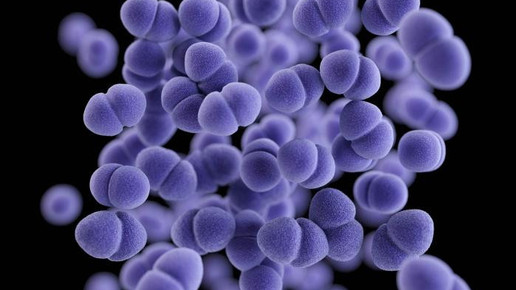
Antibiotika mit Lipopeptid-Struktur sind dafür bekannt, dass sie im Vergleich zu den meisten gängigen Antibiotika eine Arzneimittelresistenz nur sehr langsam entwickeln. Wissenschaftler der TU Berlin haben nun neue Klasse von Substanzen entdeckt, die vielversprechende Aktivitäten gegen multiresistente Bakterien – wie den Methicillin-resistenten Staphylococcus aureus (MRSA) – aufweisen. Das geht aus einer im Fachjournal „Nature Chemical Biology“ veröffentlichten Studie hervor.
Lipopeptide sind mit Lipiden modifizierte Peptide. Zu den Vertretern gehören beispielsweise das bakterizid wirksame Daptomycin (Cubicin, MSD), das intravenös appliziert wird und auch bei MRSA indiziert ist. Des Weiteren gibt es auch solche Wirkstoffe, die antimykotisch aktiv sind, dazu gehört unter anderem Caspofungin (Cancidas, MSD). Lipopeptide zeigen eine starke antimikrobielle Aktivitäten gegen ein breites Spektrum von Pathogenen und haben einen speziellen Wirkmechanismus, der die geringe Tendenz zur Resistenzausbildung erklärt.
Ein Forscherteam des Fachgebiets Biologische Chemie um Professor Dr. Roderich Süßmuth von der TU Berlin hat kürzlich aus der Klasse der Lipopeptid-Antibiotika die „Lipolanthine“ entdeckt. In Zusammenarbeit mit der französischen Firma Deinove konnten die Wissenschaftler aus einer Kultur des Bakteriums „Microbacterium arborescens“ eine Verbindung mit starker Aktivität gegen MRSA und andere pathogene Bakterien isolieren. „Bakterien und Pilze stellen eine sehr gute Quelle für bioaktive Wirkstoffe dar, denn im Wettstreit um limitierte Ressourcen bekämpfen sich Mikroorganismen in der Natur gegenseitig. Dies können wir uns zunutze machen“, erklärt Süßmuth. Die entdeckte Substanz wurde „Microvionin“ genannt und gehört zur Gruppe der „Lipolanthine“.
Zuerst analysierten die Forscher die chemische Struktur des Moleküls. Sie stellten fest, dass Microvionin aus einem Peptid- und einem Fettsäureteil besteht, wobei drei der Aminosäuren so modifiziert werden, dass sich zwei Ringstrukturen ausbilden, eine davon weist eine Thioetherbrücke auf. Aufgrund der bizyklischen Struktur wird die Verbindung zu den „Lanthipeptiden“ gezählt, einer Klasse an ribosomal synthetisierten und posttranslational modifizierten Peptiden (RiPP).
Im Anschluss konnten die Forscher zeigen, dass die Zyklisierung des Moleküls enzymatisch abläuft. So werde die Bildung von ungewünschten Nebenprodukten verhindert. „Was uns zusätzlich interessiert, ist die ziemlich ungewöhnliche Fettsäuremodifikation. Hier scheinen zum ersten Mal bei ribosomal synthetisierten Peptiden zwei Biosynthesewege zusammen zu laufen, nämlich ribosomal synthetisierte Peptide und Polyketidsynthasen, deren Zusammenspiel so bisher nicht beobachtet wurde. Das ist für uns natürlich spannend und wird weiterhin intensiv erforscht“, so Süßmuth. Zusätzlich wollten die Wissenschaftler herausfinden, ob ob es noch weitere ähnliche Verbindungen in der Natur gibt. Mithilfe des „Genome Mining“ konnten sie als zehn potenzielle Kandidaten identifizieren. Aus einem dieser Stämme (Nocardia terpenica) haben sie dann „Nocavionin“ isoliert.
Dem Wissenschaftler zufolge wird sich die Gruppe der Lipolanthine weiter vergrößern. „Wir versuchen natürlich, nun auch die anderen Moleküle zu isolieren und dann auch Rückschlüsse zwischen der Struktur und Bioaktivität zu ermitteln. Außerdem ist auch die Aufklärung der verbleibenden Schritte der Biosynthese für uns sehr interessant. Zu guter Letzt hoffen wir auch die Entwicklung von Microvionin zu einem nutzbaren Medikament vorantreiben zu können.“
Multiresistente Keime sind eine globale Bedrohung für die öffentliche Gesundheit, eine Infektion mit diesen Erregern kann für Patienten aufgrund der Resistenzen tödlich enden. Die Studienergebnisse könnten einen Beitrag dazu leisten, die Gefahr für die Bevölkerung zu reduzieren. Denn jährlich sterben mehrere Tausend Menschen an solchen Infektionen.



























APOTHEKE ADHOC Debatte