FDA: Task Force untersucht alle Sartane
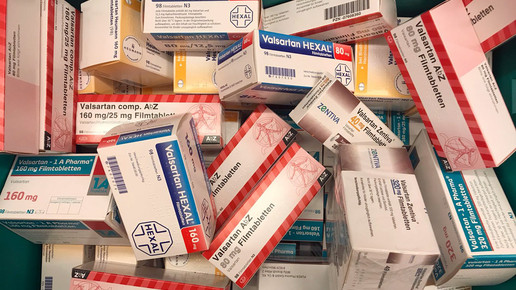
Millionen US-Amerikaner nehmen täglich ein Arzneimittel zur Blutdruckkontrolle ein, darunter auch Angiotensin-II-Rezeptor-Antagonisten wie Valsartan. Eine Task Force aus Chemikern, Toxikologen, Ärzten, Apothekern und analytischem Laborpersonal untersucht den Skandal um die als krebserregend eingestufte Verunreinigung des Wirkstoffs mit N-Nitrosodimethylamin (NDMA). Dabei sollen auch alle anderen Sartane untersucht werden.
Im Zuge der Ermittlungen zum mit NDMA belasteten Valsartan sollten verschiedene Fragen beantwortet werden. Wie viele Valsartan-haltige Arzneimittel sind betroffen? Woher stammt die Verunreinigung? Wie viele Patienten sind betroffen? Welche gesundheitlichen Risiken sind möglich? Wie können Engpässe vermieden werden? Könnten verwandte Substanzen betroffen sein?
Inzwischen konnten einige Fragen beantwortet werden. Zum einen wurde das potentielle Risiko bewertet. Die Experten schätzen, dass von 8000 Menschen, die über einen Zeitraum von vier Jahren täglich mit der maximalen Dosis von 320 mg behandelt werden, ein Patient zusätzlich an Krebs erkranken könnte. Vier Jahre, weil sich laut Schätzung der FDA verunreinigtes Valsartan solange bereits im Umlauf befindet. „Diese Schätzung repräsentierte das höchstmögliche NDMA-Expositionsniveau. Es war ein Maß für das Risiko unter den extremsten Umständen. Die meisten Patienten, die mit verunreinigtem Valsartan behandelt wurden, waren niedrigerem NDMA-Werten ausgesetzt als im Worst-Case-Szenario angenommen“, teilen die Experten mit.
Woher die Verunreinigung stammt, kann die FDA derzeit noch nicht mit voller Sicherheit sagen. „Wir sind immer noch nicht 100 Prozent sicher, was die Ursache des Problems ist“, schreibt die Behörde. Zwar könne NDMA im Zuge des Herstellungsprozesses unter bestimmten Bedingungen entstehen, doch hätten unterschiedliche Hersteller unterschiedliche Herstellungsprozesse angewendet. Außerdem sei zu klären, warum NDMA nicht bei der Aufreinigung der aktiven Substanz abgetrennt wurde.
„Sobald wir verstanden haben, wie NDMA als Nebenprodukt während des Herstellungsprozesses entsteht, werden wir sicherstellen, dass zukünftig eine Prüfung auf diese Verunreinigung erforderlich ist, wenn im Zuge der Synthese ein erhöhtes Risiko besteht.“
In einigen Fällen könnte bei der Synthese anderer Wirkstoffe der Substanzklasse aufgrund eines ähnlichen Herstellungsverfahrens ebenfalls NDMA als Verunreinigung entstehen. Daher würden auch andere Angiotensin-II-Rezeptor-Antagonisten überprüft. Die Untersuchungen würden so lange durchgeführt, bis alle Produkte identifiziert sind, die NDMA enthalten können.
NDMA zählt zu den Nitrosaminen und kann möglicherweise Krebs erzeugen. Im Tierversuch an Nagetieren wurde eine kanzerogene Wirkung auf Leber, Niere, Lunge und Blutgefäße bereits bei einer Gesamtdosis von 1 mg/kg Körpergewicht festgestellt. Bei oraler Gabe entwickelten sich vorwiegend Lebertumore. Zwar gibt es keine Daten zur Wirkung am Menschen, jedoch könne aufgrund der Gewebeähnlichkeit auf eine kanzerogene Wirkung geschlossen werden. Die Substanz methyliert die DNA-Basen Guanin und Adenin und kann auch in gepökeltem Fleisch sowie in alkoholischen Getränken vorkommen.









































APOTHEKE ADHOC Debatte