EMA: Leitlinien zur Vermeidung von Nitrosaminen
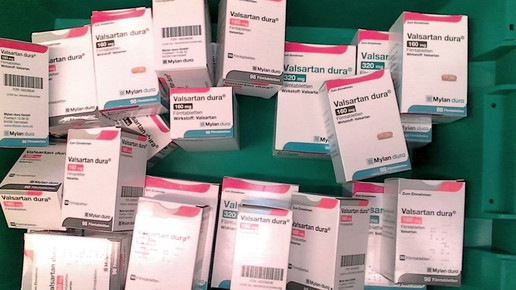
Substanzen wie N-Nitrosodimethylamin (NDMA) sind seit dem Valsartan-Skandal ein großes Thema in den Apotheken. Der Blutdrucksenker war lange Zeit nicht lieferbar. Mit den Monaten zeigte sich, dass die Vermeidung dieser Arzneimittelverunreinigungen nicht ohne weiteres möglich ist. Es wurde auch diskutiert, ob es durch längere Lagerung oder Temperatureinwirkungen zur Entstehung von Nitrosaminen kommen kann. Nun hat die Europäische Arzneimittelagentur (EMA) ein Gutachten zur Reduzierung von Nitrosaminen in Arzneimitteln verabschiedet.
Seit Sommer 2018 beeinträchtigen Nitrosamine als Verunreinigung in verschiedenen Wirkstoffen die Arzneimittelversorgung. In dem aktuellen Gutachten der EMA zur Reduzierung von Nitrosaminen in Arzneimitteln werden die Unternehmen aufgefordert Maßnahmen zu ergreifen, um das Vorhandensein dieser Arzneistoffe in Humanarzneimitteln so weit wie möglich zu begrenzen. Ebenfalls soll sichergestellt werden, dass der Gehalt an diesen Verunreinigungen die strengen Grenzwerte nicht überschreitet. Zuletzt wurden immer wieder einzelne Chargen von Valsartan & Co. aufgrund unzureichender Spezifikationswerte zurückgerufen.
Die Maßnahmen sind wichtig, da Nitrosamine potenziell kanzerogen sind. Grundsätzlich sollen Patienten keinem zusätzlichen Lebenszeitrisiko für eine Krebserkrankung von mehr als 0,001 Prozent durch Nitrosamine in Arzneimitteln ausgesetzt werden. Somit soll die Leitlinie sicherstellen, dass Nitrosamine in den künftigen Arzneimittelchargen entweder nicht vorhanden sind oder unterhalb der ermittelten Grenzwerte liegen. „Die Unternehmen werden verpflichtet über geeignete Kontrollstrategien zu verfügen, die das Vorhandensein dieser Verunreinigungen verhindern oder begrenzen. Falls erforderlich sind die Herstellungsverfahren entsprechend zu verbessern“ heißt es in der Mitteilung.
Nähere Informationen folgen
Inwiefern die Prozesse umgestellt werden könnten, ist nicht näher beschrieben – die Prozessoptimierung obliegt dem einzelnen Hersteller. Nitrosamine könnten immer wieder auftreten, um das Risiko einer Spezifikationsabweichung beurteilen zu können, verweist die EMA darauf, dass regelmäßig Tests durchzuführen sind, um das Vorhandenseins von Nitrosaminen zu detektieren. Bisher steht nur das Gutachten zur Vermeidung der Nitrosamine. Das grobe Gerüst steht also. Detaillierte Informationen für Unternehmen, einschließlich der Fristen, sollen bald als Download auf der Nitrosamin-Webseite der EMA zur Verfügung stehen. Bis dahin gelten die aktuellen Anweisungen – Unternehmen könnten sich bis zur Veröffentlichung an den bereits zur Verfügung gestellten Dokumenten orientieren.
Nicht alle Unternehmen folgten den Anweisungen
Im Zuge eines Risikobewertungsverfahrens auf europäischer Ebene wurden die pharmazeutischen Unternehmen im April vergangenen Jahres aufgefordert, das Herstellungsverfahren von Sartanen, die eine Tetrazol-Gruppe enthalten, zu überprüfen, um das Auftreten von Nitrosaminen zu vermeiden. Der Verpflichtung sind jedoch nicht alle pharmazeutischen Unternehmen nachgekommen. Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) drohte Anfang des Jahres folglich mit dem Ruhen der Zulassung. Denn seit dem Skandal müssen die Hersteller sicherstellen, dass die potentielle Bildung von Nitrosaminen im Herstellungsprozess überprüft und – wenn nötig – geändert wird. Hierfür gilt eine Übergangsfrist von zwei Jahren.
Grenzwerte für zweijährige Übergangsfrist
- Valsartan 320 mg:
- NDEA 26,5 ng/Tag und 0,082 ppm in der API und NDMA 96 ng/Tag und 0,300 ppm in der API
- Losartan 150 mg:
- NDEA 26,5 ng/Tag und 0,177 ppm in der API und NDMA 96 ng/Tag und 0,640 ppm in der API
- Olmesartan 40 mg:
- NDEA 26,5 ng/Tag und 0,663 ppm in der API und NDMA 96 ng/Tag und 2,400 ppm in der API
- Irbesartan 300 mg:
- NDEA 26,5 ng/Tag und 0,088 ppm in der API und NDMA 96 ng/Tag und 0,320 ppm in der API
- Candesartan 32 mg:
- NDEA 26,5 ng/Tag und 0,820 ppm in der API und NDMA 96 ng/Tag und 3,000 ppm in der API
Auch Metformin und Ranitidin betroffen
Nicht nur die Sartane, sondern auch Metformin und Ranitidin sind von Nitrosamin-Verunreinigungen betroffen: So hatte die EMA die Zulassungsinhaber Anfang März in die Pflicht genommen, alle Produkte mit chemisch synthetischen Wirkstoffen zu überprüfen und deren Risiko auf die potenzielle Verunreinigung mit einem Nitrosamin zu bewerten. Patienten wurden angehalten, metforminhaltige Arzneimittel wie gewohnt weiterhin einzunehmen. „Das Risiko einer unzureichenden Behandlung eines Diabetes überwiegt bei weitem die möglichen Risiken, die sich aus der Aufnahme geringer Nitrosamin-Konzentrationen ergeben.“ Metformin gilt als kritisches Medikament. Daher arbeiten EMA und nationale Behörden eng zusammen, um mögliche Versorgungsengpässe zu vermeiden. Das H2-Antihistaminikum Ranitidin sollten Ärzte und Apotheker zuletzt zur Behandlung von Sodbrennen und Magengeschwüren nicht mehr empfehlen. Da Nitrosamine in zahlreichen Präparaten oberhalb der Grenzwerte gefunden wurden, ohne dass die Quelle der Verunreinigungen bekannt war, sollten die Präparate laut EMA vorerst nicht mehr eingenommen werden. In den USA hatte die Arzneimittelbehörde FDA bereits vier Wochen zuvor zur Marktrücknahme aufgefordert.




















APOTHEKE ADHOC Debatte