Lunapharm: Qualität der beschlagnahmten Proben bestätigt
Es ist so weit, der abschließende Untersuchungsbericht der Task Force im Fall Lunapharm liegt vor. Die Labor-Ergebnisse der 39 bei Lunapharm oder dem Transportunternehmen beschlagnahmten Proben sind in den Bericht eingeflossen. Das Ergebnis ist klar: „Bei keiner der untersuchten Proben wurde die Qualität der Medikamente beanstandet.“ Einzig die bereits im Januar 2016 abgelaufene Rückstellprobe zeigte geringfügige Abweichungen.
„Die vorliegenden Laborergebnisse geben keine Hinweise auf eine verminderte pharmazeutische Qualität der betroffenen Arzneimittel“, teilt das Ministerium für Arbeit, Soziales, Gesundheit, Frauen und Familie des Landes Brandenburg mit. „Die Wahrscheinlichkeit, dass Patientinnen und Patienten dem Risiko einer gesundheitliche Schädigung ausgesetzt waren, ist damit sehr gering, kann aber gleichwohl nicht völlig ausgeschlossen werden,“ räumt die Behörde ein.
Im Bericht der Task Force ist zu lesen, dass für drei Rückstellmuster – Lucentis, Avastin und MabThera – bisher keine laboranalytischen Untersuchungen vorgenommen werden konnten, da diese noch beim LKA Brandenburg verwahrt werden. Alle untersuchten Proben wurde die Qualität bestätigt und keine Mängel dokumentiert. Untersucht wurden die Proben in unterschiedlichen Laboren, darunter staatliche Untersuchungslabors (OMCL) und der Firma Roche.
Am Institut für pharmazeutische und angewandte Analytik in Bremen wurden sechs Proben analysiert – Alimta 500mg Pulver zur Herstellung einer Infusionslösung in den Chargen C 749717E (Verfalldatum 03/2020), C445327C (Verfalldatum 02/2018) und C556499F (Verfalldatum 01/2019) sowie Velcade 3.5mg Pulver zur Herstellung einer Injektionslösung in den Chargen GCZTQ00 (Verfalldatum 02/2019), FIZSW01 (Verfalldatum 08/2018) und FEZUB00 (Verfalldatum 04/2018). Das Augenmerk lag sowohl auf den äußeren Umhüllungen als auch auf dem Inhalt in Bezug auf Wirkstoffgehalt und dem Gehalt möglicher Verunreinigungen. „Alle Proben der Arzneimittel Alimta und Velcade wiesen keine Mängel hinsichtlich der Spezifikationen für die untersuchten Parameter auf“, schreibt die Task Force.
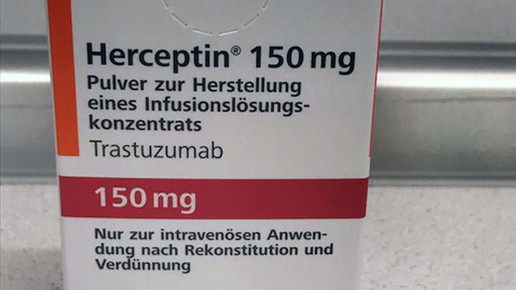
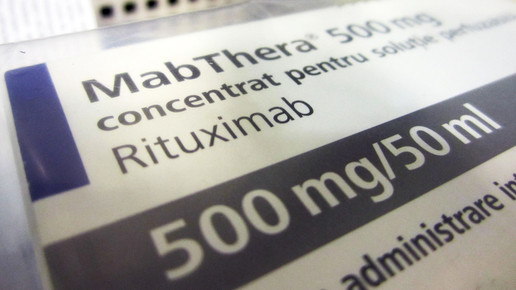
Roche untersuchte insgesamt 22 Arzneimittel, die am 22. und 24. Juli beschlagnahmt wurden – drei proben Avastin, zehn Proben Herceptin und neun Proben MabThera. „Die chemisch-physikalischen Untersuchungen ergaben, dass alle Proben hinsichtlich der Identität der Wirkstoffe den Anforderungen dem Originalmaterial der Firma Roche entsprachen. Dies wurde auch für den Gehalt und die Reinheit (Abwesenheit von Verunreinigungen des Wirkstoffes innerhalb der zulässigen Grenze) festgestellt.“ Auffällig war lediglich eine probe Herceptin, die jedoch bereits im Januar 2016 abgelaufen war. Die Analysen zeigten eine höheren Gehalt an Verunreinigungen, „diese Packung hätte in keinem Fall an Patienten verabreicht werden dürfen.“
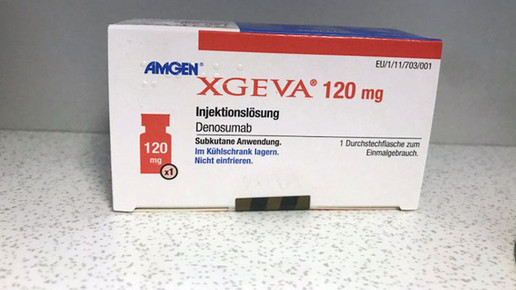
Das Bayerische Landesamt für Gesundheit und Lebensmittelsicherheit (LGL) in Oberschleißheim untersuchte vier Proben Xgeva in unterschiedlichen Chargen. „Alle vier Proben entsprachen hinsichtlich Identität und Gehalt des Wirkstoffes den Anforderungen des pharmazeutischen Unternehmers. Hinweise auf nicht den Spezifikationen entsprechende Veränderungen des Wirkstoffes ergaben sich nicht. Obwohl die Sicherheitssiegel der Umverpackungen geöffnet waren, waren die enthaltenen Behältnisse (Vials) unversehrt.“
Abschließend schreibt die Task Force, dass die Wahrscheinlichkeit sehr gering sei, dass bei Patienten Arzneimittel mit einer unzureichenden pharmazeutischen Qualität angewendet wurden und sie dadurch einem Risiko für eine gesundheitliche Schädigung ausgesetzt waren.“ Die Aussage beziehe sich jedoch nur auf die Arzneimittel derselben Chargen, von denen die Rückstellmuster laboranalytisch untersucht wurden.
Für die heute zur neuen Ministerin für Arbeit, Soziales, Gesundheit, Frauen und Familie des Landes Brandenburg ernannte Susanna Karawanskij hat die Task Force Lunapharm „eine sehr gute und hilfreiche Arbeit geleistet.“ Der Bericht werde maßgeblich zur Aufarbeitung des Skandals beitragen, so die frischgebackene Ministerin, für die die Sicherheit der Patienten oberste Priorität hat. „Im Ministerium wird ein neues Referat geschaffen, das sich ausschließlich um die Arzneimittelaufsicht kümmern soll. Außerdem werden wir wieder ein Controlling-System installieren, um interne Abläufe kontinuierlich zu prüfen und zu verbessern. Wenn es um Patienteninteressen geht, dürfen Maßnahmen nicht im Verwaltungsgeschehen versanden. Wo Gefahr im Verzug ist, muss umgehend gehandelt werden,“ so Karwanskij.
Die Ministerin spricht von einem europaweit agierenden Netzwerk, das mit einem offenbar hohen Maß an krimineller Energie illegalen Arzneimittelhandel betreibe. „Die gesetzliche Importquote für Arzneimittel gehört auf den Prüfstand. Durch das System aus Reimporten und Parallelimporten sind höchst verschachtelte Handelsbeziehungen zwischen Herstellern, Großhändlern und Zwischenhändlern entstanden, welche die Arzneimittelaufsichten der Länder vor enorme Herausforderungen stellen“, betont Karwanskij.
Dem Landesamt für Arbeitsschutz, Verbraucherschutz und Gesundheit (LAVG) sind derzeit sieben Brandenburger Apotheken bekannt, die Arzneimittel der zurückgerufenen Chargen bezogen und an Patienten abgegeben haben. Man wisse aktuell von mindestens elf Betroffenen, die mit den zurückgerufenen Arzneimitteln, die Lunapharm vor der griechischen Apotheke bezogen haben soll, behandelt wurden.












































APOTHEKE ADHOC Debatte