Lunapharm: AMK ruft Geisterware zurück
Schmuggelware muss zurück: Aufgrund von Unstimmigkeiten in der Lieferkette ruft Lunapharm diverse Arzneimittel in verschiedenen Chargen zurück. Die Auslieferung der betroffenen Arzneimittel erfolgte vom 14. September 2015 bis zum 6. April 2017.
Alimta 500 mg, Lunapharm, 1 Stück, Pulver zur Herstellung eines Infusionslösungskonzentrats, Ch.-B.: C556500E, interne Reg.-Nr.: 16102GR
Herceptin 150 mg, Lunapharm, 1 Stück, Pulver zur Herstellung eines Infusionslösungskonzentrats, diverse Chargen
Mabthera 100 mg, Lunapharm, 2 Stück, Infusionslösungskonzentrat, Ch.-B.: N7114B20, interne Reg.-Nr.: 17017GR
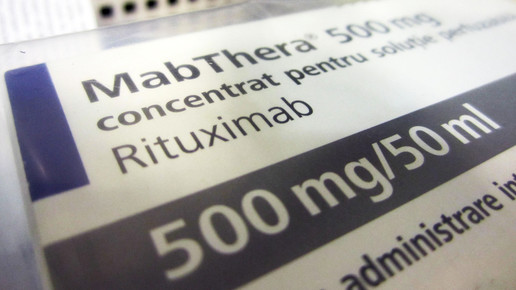
Mabthera 500 mg, Lunapharm, 1 Stück, Infusionslösungskonzentrat, diverse Chargen
Velcade 3,5 mg, Lunapharm, 1 Stück, Pulver zur Herstellung einer Infusionslösung, diverse Chargen
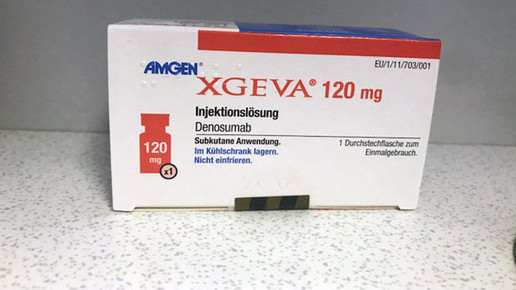
Xgeva 120 mg, Lunapharm, 1 Stück, Injektionslösung, diverse Chargen
Lunapharm Deutschland mit Sitz in Mahlow ruft alle noch in der Laufzeit befindlichen Arzneimittel zurück, die vom griechischen Lieferanten Pharmacy Ozbagdzi haralampidis Stilianos bezogen wurden. Es handele sich um einen vorsorglichen Rückruf, denn derzeit gebe es keine Hinweise auf eine Patientengefährdung. Es bestehe jedoch der Verdacht, dass die betroffenen Arzneimittel in griechischen Krankenhäusern gestohlen wurden und deren Lager- und Transportbedingungen möglicherweise nicht den Anforderungen entsprachen.
Der Rückruf wird vom LAVG Brandenburg überwacht. Apotheker werden gebeten, das Warenlager zu überprüfen. Lagerbestände mit den genannten Chargen und dazugehörigen internen Registriernummern sollen in Quarantäne gestellt werden. Die Abholung ist unter der Telefonnummer 03379 370139 anzumelden. Die Auslieferung der betroffenen Arzneimittel erfolgte vom 14. September 2015 bis zum 6. April 2017.
Betroffen sind folgende Arzneimittel:
- Alimta 500 mg, Lunapharm, 1 Stück, Pulver zur Herstellung eines Infusionslösungskonzentrats, Ch.-B.: C556500E, interne Reg.-Nr.: 16102GR
- Herceptin 150 mg, Lunapharm, 1 Stück, Pulver zur Herstellung eines Infusionslösungskonzentrats, Chargen H4476B02, interne Reg.-Nr.: 16041GR, H4544H02, interne Reg.-Nr.: 15090FR,, H4586H04, interne Reg.-Nr.: 16030GR, H4724H02, interne Reg.-Nr.: 16099GR, N1028B02, interne Reg.-Nr.: 15-0052-GR. N1028B03, interne Reg.-Nr.: 15115GR, N1033B02, interne Reg.-Nr.: 15102GR, N1033B02, interne Reg.-Nr.: 15114GR, N1048H01, interne Reg.-Nr.: 16083FR
- Mabthera 100 mg, Lunapharm, 2 Stück, Infusionslösungskonzentrat, Ch.-B.: N7114B20, interne Reg.-Nr.: 17017GR
- Mabthera 500 mg, Lunapharm, 1 Stück, Infusionslösungskonzentrat, Chargen: N7112B02, interne Reg.-Nr.: 17103FR, N7113B04, interne Reg.-Nr.: 16107GR, N7113B06, interne Reg.-Nr.: 17037IT, N7117B08, interne Reg.-Nr.: 16082FR, N7119B08, interne Reg.-Nr.: 17021GR, N7120B08, interne Reg.-Nr.: 17023GR, N7121B02, interne Reg.-Nr.: 16087FR, N7122B03, interne Reg.-Nr.: 16094FR
- Velcade 3,5 mg, Lunapharm, 1 Stück, Pulver zur Herstellung einer Infusionslösung, Chargen: GBZSR00, interne Reg.-Nr.: 17029GR, GCZTQ00, interne Reg.-Nr.: 17014GR, FIZSW01, interne Reg.-Nr.: 16090GR, FIZSX00, interne Reg.-Nr.: 17030GR
- Xgeva 120 mg, Lunapharm, 1 Stück, Injektionslösung, Chargen: , 1066962A, interne Reg.-Nr.: 17011FR, 1069054A, interne Reg.-Nr.: 17009FR, 1069061A, interne Reg.-Nr.: 17010FR, 1070161A, interne Reg.-Nr.: 17008FR, 1071480A, interne Reg.-Nr.: 17012GR
Weitere AMK-Meldungen:
Buparid 0,25 mg Suspension für einen Vernebler, 20x2 ml, 40x2 ml und 60x2 ml, alle Chargen
Buparid 0,5 mg und 1 mg Suspension für einen Vernebler, 20x2 ml, 40x2 ml, 60x2 ml und 60x2 ml mit Vernebler, alle Chargen
Im Rahmen von Stabilitätsuntersuchungen wurden bei einer Charge eine Abweichung von der Spezifikation – Impurity L – festgestellt. Weitere Chargen befinden sich an der oberen Grenze. Bislang liegen keine Hinweise auf eine Patientengefährdung vor, dennoch erfolge ein vorsorglicher Rückruf. Da die Einhaltung der Spezifikation für Impurity L nicht sicher bis zum angegebenen Verfallsdatum garantiert werden könne, wird der Vertrieb aller Wirkstärken des Produktes Buparid Suspension für einen Vernebler zum 31. Juli 2018 eingestellt. In diesem Zusammenhang werden etwaige noch im Handel befindliche Packungen zurückgerufen.
Apotheker werden gebeten, das Warenlager zu überprüfen. Lagerbestände sind bis zum 31. August an den Großhandel zurückzuschicken.











































APOTHEKE ADHOC Debatte