Nagelpilz: Neue Behandlungsoption ab Mai
Ab Mai steht mit Jublia (Efinaconazol, Almirall) ein topisches Triazol-Antimykotikum zur täglichen Behandlung von leichter bis mittelschwerer Onychomykose in Deutschland zur Verfügung. Das Präparat wird über 48 Wochen angewendet und ist für Patientinnen und Patienten ab sechs Jahren auf Privatverordnung erhältlich. Die Zulassung stützt sich auf Phase-III-Studien, deren Ergebnisse eine Wirksamkeit in der Größenordnung von oralen Itraconazol-Therapien aufzeigen.
Efinaconazol ist ein spezifisch zur Therapie der Onychomykose entwickeltes topisches Triazol-Antimykotikum. Nach der Marktetablierung in den USA, Kanada und dem asiatischen Raum erfolgt ab Mai die Einführung in Deutschland unter dem Handelsnamen Jublia. Bereits im Jahr 2022 kündigte Almirall diesen Schritt nach dem Erwerb der europäischen Lizenzrechte an.
Behandlung über 48 Wochen
Das Präparat ist für die äußerliche Behandlung von leichter bis mittelschwerer Onychomykose der Zehennägel ohne Matrixbeteiligung zugelassen. Die Anwendung ist für Patient:innen ab sechs Jahren möglich und erfolgt über 48 Wochen einmal täglich.
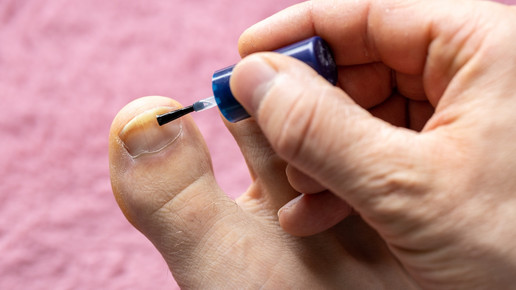
Mithilfe des integrierten Durchflusspinsels wird die Lösung auf die betroffenen Nägel aufgetragen. Ein Anfeilen oder die Nutzung von Lösungsmitteln sind nicht erforderlich ist. Die Applikation sollte laut Hersteller idealerweise abends vor dem Schlafengehen erfolgen, um eine ausreichende Einwirkzeit über Nacht zu gewährleisten.
„Jublia ist verschreibungspflichtig, aber nicht erstattungsfähig“, erklärt Almirall. Die Verordnung der Mehrfachpackung mit zwei Flaschen zu je 4 ml sei deshalb nur privat möglich.
Geringere Bindungsaffinität zu Keratin
Die pharmakologische Wirkung resultiert aus der kompetitiven Hemmung der Lanosterol-14-alpha-Demethylase, einem Schlüsselenzym der Ergosterol-Biosynthese. Der daraus entstehende Ergosterolmangel führt zu einer gesteigerten Membranpermeabilität und irreversiblen degenerativen Veränderungen der Pilzzelle. Das Wirkspektrum deckt die klinisch relevanten Erregergruppen der Dermatophyten, Hefen und Schimmelpilze ab.
Ein wesentliches pharmakokinetisches Merkmal ist das Diffusionsverhalten von Efinaconazol durch die menschliche Nagelplatte. Im Vergleich zu anderen topischen Antimykotika weist das Molekül eine deutlich geringere Bindungsaffinität zu Keratin auf. Da der Wirkstoff nicht fest an die Proteinmatrix des Nagels gebunden wird, verbleibt ein höherer Anteil in freier, aktiver Form.
Die 10-prozentige Lösung durchdringt die gesamte Nageldicke. Dadurch gelangt der Wirkstoff in das Nagelsubstrat sowie das Nagelbett und erreicht auch tiefer liegende Bereiche oder Hohlräume.
Beurteilung der klinischen Wirksamkeit
Zwei klinische Phase-III-Studien über 52 Wochen prüften die Wirksamkeit bei 1655 Patient:innen im Alter von 18 bis 70 Jahren mit 20 bis 50 Prozent Nagelbefall. Vier Wochen nach Therapieende ermittelten die Forschenden die vollständige Heilung als primären Endpunkt.
Jublia schnitt in allen Endpunkten statistisch signifikant besser ab als das wirkstofffreie Vehikel. Eine komplette Heilung erreichten 15,2 bis 17,8 Prozent der Teilnehmenden, eine mykologische Heilung 53,4 bis 55,2 Prozent. Diese Ergebnisse entsprechen der Größenordnung von oralem Itraconazol, wobei dessen Studien auch die Nagelmatrix einschlossen. Direkte Vergleichsstudien zwischen beiden Therapien fehlen jedoch.
Die beiden Phase-III-Zulassungsstudien mit dem Titel „Efinaconazole 10% solution in the treatment of toenail onychomycosis: Two phase III multicenter, randomized, double-blind studies“ wurden an 118 Standorten in den USA, Kanada und Japan durchgeführt und im Jahr 2013 im Fachmagazin Journal of the American Academy of Dermatology veröffentlicht. Obwohl die Studien ursprünglich von Valeant Pharmaceuticals und Kaken Pharmaceutical finanziert wurden, ist Almirall seit 2021 durch einen Lizenzvertrag der Inhaber der exklusiven Vermarktungsrechte für Europa und nutzt diese Daten heute als offizielle Basis für die europäische Zulassung.

APOTHEKE ADHOC Debatte