NMBA: FDA legt Grenzwert fest
Im Februar wurden in Deutschland und den USA Losartan-haltige Arzneimittel aufgrund einer Verunreinigung mit dem Nitrosamin N-Nitroso-N-methyl-4-Aminobuttersäure (NMBA) zurückgerufen. Die betroffenen Chargen enthalten die von Hetero Labs Limited produzierte aktive Substanz. Der indische Lohnhersteller selbst hatte die Verunreinigung im Blutdrucksenker identifiziert. Zum Monatsanfang hatte die US-Arzneimittelbehörde FDA eine Risikobewertung und einen Grenzwert für NMBA veröffentlicht.
Ende Februar rief Camber Pharmaceuticals 87 Chargen Losartan-haltiger Arzneimittel zurück. Betroffenen waren die Wirkstärken 25, 50 und 100 mg, die mit der aktiven Substanz aus der Produktion von Hetero Labs hergestellt wurden. Die enthaltene Verunreinigung NMBA wird von der Weltgesundheitsorganisation (WHO) für den Menschen als potenziell krebserregend eingestuft und ist nach N-Nitrosodimethylamin (NDMA) und N-Nitrosodiethylamin (NDEA) das dritte Nitrosamin, das für weltweite Rückrufe verschiedener Sartane verantwortlich ist.
Am 3. März hatte Torrent Pharmaceuticals in den USA 114 Chargen Losartan-haltiger und Losartan/Hydrochlorothiazid-haltiger Arzneimittel zurückgerufen. Auch hier lag die NMBA-Konzentration außerhalb der zulässigen Spezifikation. Die API stammt ebenfalls aus der Produktion von Hetero Labs (die Substanz, der für deutschen Markt bestimmten Heumann-Produkte stammt ebenfalls vom indischen Lohnhersteller). Beide, Torres und Camber, haben Arzneimittel zurückgerufen, deren NMBA-Konzentration über dem zwischenzeitlich akzeptablen Grenzwert von 0,96 ppm lag.
Die FDA hat die zurückgerufenen Arzneimittel untersucht und NMBA-Konzentrationen außerhalb des akzeptablen Grenzbereichs bestätigt. Die Behörde vermutet, dass die Verunreinigung während des Herstellungsprozesses beispielsweise durch bestimmte Chemikalien oder Reaktionsbedingungen anfällt oder durch die Wiederverwendung bestimmter Materialien oder Lösungsmittel in die API gelangt. In den zuvor zurückgerufenen Sartan-haltigen Arzneimittel konnte NMBA nicht als Verunreinigung identifiziert werden.
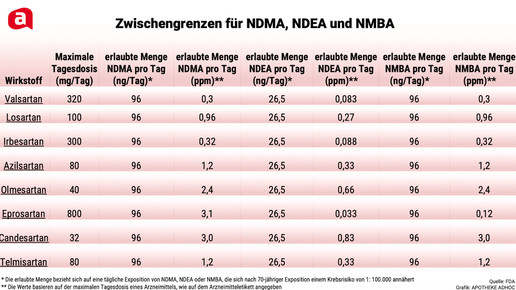
Ende Februar hat die FDA eine Tabelle mit den zulässigen Grenzwerten für NMDA, NDEA und NMBA veröffentlicht. Diese soll den Herstellern helfen, freiwillige Rückrufe zu initiieren. Zudem weist die Behörde darauf hin, dass in Zusammenarbeit mit der Industrie und den internationalen Aufsichtsbehörden alles getan werde, dass Sartane, die auf den Markt kommen, frei von Verunreinigungen sind. Allerdings würden kurzzeitig Verunreinigungen unterhalb der festgelegten Grenzwerte toleriert, um einem Lieferengpass entgegenzuwirken.
Das sind die Grenzwerte:
- Valsartan 320 mg: NDMA und NMBA je 96 ng/d (0,3 ppm), NDEA 26,5 ng/d (0,083 ppm)
- Losartan 100 mg: NDMA und NMBA je 96 ng/d (0,96 ppm), NDEA 26,5 ng/d (0,27 ppm)
- Irbesratan 300 mg: NDMA und NMBA je 96 ng/d (0,32 ppm), NDEA 26,5 ng/d (0,088 ppm)
- Azilsartan 80 mg: NDMA und NMBA je 96 ng/d (1,2 ppm), NDEA 26,5 ng/d (0,33 ppm)
- Olmesartan 40 mg: NDMA und NMBA je 96 ng/d (2,4 ppm), NDEA 26,5 ng/d (0,66 ppm)
- Eprosartan 800 mg: NDMA und NMBA je 96 ng/d (0,12 ppm), NDEA 26,5 ng/d (0,033ppm)
- Candesartan 32 mg: NDMA und NMBA je 96 ng/d (3,0 ppm), NDEA 26,5 ng/d (0,83ppm)
- Telmisartan 80 mg: NDMA und NMBA je 96 ng/d (1,2 ppm), NDEA 26,5 ng/d (0,33ppm).
Wer täglich bei der maximalen Dosierung der einzelnen Sartane 96 ng NDMA oder NMBA beziehungsweise 26,5 ng NDEA über einen Zeitraum von 70 Jahren zu sich nimmt, hat laut FDA ein zusätzliches Krebsrisiko von 1:100.000. „Wir sind zutiefst besorgt über die Anwesenheit eines dritten Nitrosamins in bestimmten Sartanen. Es muss jedoch betont werden, dass das erhöhte Krebsrisiko bei Patienten mit NMBA-Exposition auf der Grundlage der ersten Einschätzung der FDA für eine NDMA-Exposition das gleiche zu sein scheint – aber geringer als bei NDEA“, schreibt die US-Behörde.

















APOTHEKE ADHOC Debatte