Covid: Antikörper-Cocktail von Regeneron zugelassen
Die US-Arzneimittelbehörde FDA hat dem Antikörper-Cocktail von Regeneron zur Behandlung von Covid-19 in den USA eine Notfallzulassung erhalten.
Damit kann der Cocktail mit zwei Antikörpern zur Behandlung von Patienten ab zwölf Jahren eingesetzt werden, bei denen das Risiko besteht, dass sie schwere Covid-19-Symptome entwickeln. Patienten, die sich im Krankenhaus befinden oder Sauerstoff benötigen, dürfen das Medikament nicht bekommen.
Die FDA erteilte die Zulassung nach einer klinischen Studie mit 799 Erwachsenen mit leichten bis mittelschweren Covid-19-Symptomen, die nicht im Krankenhaus waren. Nach Angaben der „New York Times“ erhielt Regeneron von der US-Regierung mehr als 500 Millionen Dollar für die Entwicklung des Medikaments. Die ersten 300.000 Dosen werden von der Regierung kostenlos zur Verfügung gestellt, aber die Patienten müssen möglicherweise Kosten an Gesundheitseinrichtungen zahlen, um das Medikament verabreicht zu bekommen, teilte der Arzneimittelhersteller in einer Erklärung mit.
Reduzierung der Viruslast
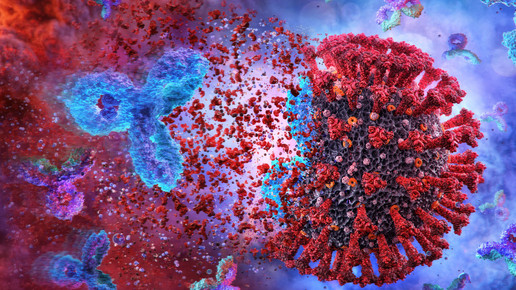
Der Antikörper-Cocktail soll verhindern, dass das Virus in die Zelle eintreten kann. Die Behandlung führt dem Unternehmen zufolge zu einer Reduzierung der Viruslast, also der Menge an nachweisbaren Viren, und zu einem rascheren Abklingen der Symptome. Am stärksten profitierten demnach diejenigen Probanden, deren Immunsystem noch keine eigenen Antikörper gegen das Virus gebildet hatte. Die Antikörper richten sich gegen zwei Regionen des Spike-Proteins auf der Oberfläche des Sars-CoV-2-Virus.
Nach seiner Genesung von Covid-19 hatte Trump im Oktober für die Behandlung der Krankheit mit dem Antikörper-Cocktail von Regeneron geworben. Das Medikament sei keine Behandlungsmethode, sondern ein „Heilmittel“ und ein „Wunder“, das bald allen zur Verfügung stehen solle, hatte er versprochen.
Nicht der erste zugelassene Antikörper
Erst kürzlich hatte ein anderer Antikörper die erste Notfallzulassung durch die FDA erhalten: Bamlanivimab (Lilly) kann bei Patienten mit leichten und mittelschweren Verläufen von Covid-19 eingesetzt werden. Lilly will bis Ende des Jahres bis zu eine Million Dosen des Medikaments bereitstellen.
Die Notfallzulassung umfasst den Einsatz des Antikörpers bei Erwachsenen und Kindern ab zwölf Jahren und einem Körpergewicht von mindestens 40 kg. Die Infektion muss vor der Behandlung mit Bamlanivimab durch einen positiven Test bestätigt werden. Außerdem ist der Einsatz auf solche Patienten begrenzt, bei denen ein hohes Risiko für einen schweren Verlauf mit Hospitalisierung besteht. Patienten mit einem schweren Verlauf, hospitalisierte oder beatmete Patienten dürfen nicht behandelt werden.
Es wird empfohlen, die Therapie schnellstmöglich zu beginnen – innerhalb von zehn Tagen nach Auftreten der ersten Symptome. Denn monoklonale Antikörper erzielen nach derzeitigen Erkenntnissen ihre beste Wirkung in der Frühphase von Covid-19 indem sie die Replikation von Sars-CoV-2 unterbinden.














APOTHEKE ADHOC Debatte