Gabelmann kritisiert „dürftige“ Antworten
Als „dürftig“ bezeichnet Sylvia Gabelmann, Sprecherin für Arzneimittelpolitik und Patientenrechte der Linken im Bundestag, die Antworten der Bundesregierung auf ein Kleine Anfrage zur Valsartan-Verunreinigung. 28 Fragen hatte die Fraktion an die Bundesregierung gerichtet. Viel schlauer ist man nicht geworden. Nur so viel: Eine Inspektion in Drittländern ist zumindest in der Theorie möglich.
„Es ist schon seit vielen Jahren bekannt, dass die Kontrollen bei den Arzneimittel-Produktionsstätten zum Beispiel in China oder Indien völlig unzureichend sind. Dennoch hat die Bundesregierung bislang keinerlei Verbesserung der Überwachung zustande gebracht, weder zusammen mit den europäischen Partnerländern noch durch bessere Abstimmung und mehr Personal bei den Länderbehörden“, kritisiert Gabelmann.
Die Politikerin, von Hause aus Apothekerin, geht mit der Bundesregierung streng ins Gericht. Denn auf ihre Frage, ob ein Kontrollversagen vorliege, geht die Antwort nicht ein: „Die Anforderungen an den Import von Wirkstoffen zur Arzneimittelherstellung aus Drittländern sind europäisch harmonisiert“, heißt es von der Bundesregierung Das Arzneimittelgesetz (AMG) sehe jedoch bei bestimmten Wirkstoffen eine Inspektion einer deutschen oder europäischen Behörde im Drittland vor. Der Skandal um den verunreinigten Wirkstoff macht laut Gabelmann aber deutlich: „Diese Kontrollen sind völlig unzureichend, finden zu selten oder vor Ort gar nicht statt.“ Theoretisch reicht eben nicht.
„Wie die Bundesregierung angesichts der Vorfälle mit Valsartan oder auch Lunapharm zu dem Schluss kommt, dass die Kompetenzverteilung zwischen den Behörden von Bund und Ländern sich grundsätzlich bewährt hätte, bleibt wohl ihr persönliches Geheimnis. Eine Bündelung der Befugnisse und bessere Ausstattung der Überwachungsbehörden wären wohl die mindesten Maßnahmen, die dringlich in die Wege geleitet werden müssten“, so Gabelmann weiter. Der chinesische Lohnhersteller Zhejiang Huahai Pharmaceutical hatte für die aktive Substanz beim European Directorate for the Quality of Medicines and Healthcare (EDQM) ein entsprechendes Certficate of Suitabililty (CEP) beantragt. Dieses wurde auch nach der Umstellung der Synthese genehmigt.
„Bei Syntheseänderungen werden auch neue Verunreinigungen in Betracht gezogen. N-Nitrosodimethylamin (NDMA) ist eine Verunreinigung, die nach Aussage des EDQM nicht zu erwarten war. […] Als eine erste Konsequenz ist die Anpassung der Valsartan-Monographie durch das EDQM vorgesehen“, heißt es in der Antwort auf die Anfrage. Der chinesische Hersteller habe somit nicht gegen geltendes Recht verstoßen – zumindest liegen der Bundesregierung „derzeit keine diesbezüglichen Erkenntnisse vor“.
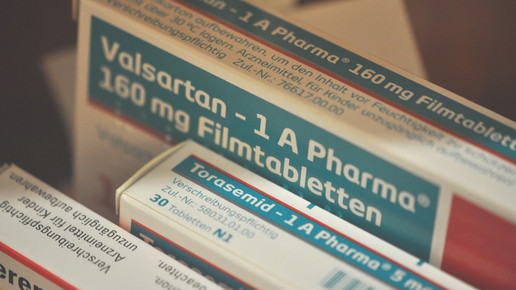
Schätzungsweise 900.000 Patienten wurden mit verunreinigtem Valsartan behandelt. Eine akute Gesundheitsgefährdung besteht laut Bundesregierung nicht. Bedeutsam seien Dauer und Menge der Aufnahme. Für Gabelmann eine fragwürdige Einschätzung: „Dabei gibt es für ein langfristiges Krebs-Risiko keinerlei Grenzwert und keinerlei Untergrenzen, bis zu denen die Aufnahme von NDMA unschädlich ist, wie die Bundesregierung auf meine Frage hin bestätigte.“
Gabelmann weiter: „Die Bundesregierung leistet den Betroffenen auch sonst keine Unterstützung: Weder führt sie eine regelhafte Erstattung der Zuzahlung ein, wenn diese bei Umstellung auf ein anderes Präparat erhoben würde. Ein Extra-Krebs-Screening für die Valsartan-Opfer will die Bundesregierung auch nicht anbieten. Ebenfalls ist nichts zu hören von unterstützenden Gutachten für die Betroffenen, die auch wegen möglicher Entschädigungsleistungen hilfreich sein könnten“, so Gabelmann weiter.
Für die Kommunikationsstrategie hat die Bundesregierung lobende Worte. „Mit einem Rückruf auf Apothekenebene wird sichergestellt, dass keine weiteren Arzneimittelpackungen, die ein verunreinigtes Arzneimittel enthalten, zu den Patientinnen und Patienten gelangen.“
Die Fraktion wollte zudem wissen, wie hoch der Anteil in Deutschland vermarkteter Arzneimittel ist, deren Wirkstoff aus China oder Indien stammt. Antwort Fehlanzeige, denn der Bundesregierung liegen keine detaillierten Informationen vor. Es sei jedoch davon auszugehen, dass insbesondere generische Arzneimittel in Drittländern – vorrangig in Indien und China – produziert würden. Den Preisdruck sieht die Bundesregierung jedoch nicht als Ursache für die Verlagerung der Wirkstoffproduktion nach Fernost. Dies sei vielmehr eine „weltweit stattfindende wirtschaftliche Entwicklung, die im Bereich der chemischen Herstellung seit vielen Jahren beobachtet werden kann.“ Ursachen seinen vielmehr niedrigere Investitionskosten und günstigere Arbeitskosten.
Bundesgesundheitsminister Jens Spahn hat angekündigt, die Arzneimittelüberwachung auf den Prüfstand zu stellen: „Einen Arzneimittelrückruf können wir – selbst mit Erkenntnissen wie bei Valsartan – gar nicht starten von Bundesebene, das können nur 16mal die Länder jeweils.“ Deswegen prüfe man, inwieweit Gesetzesänderungen nötig seien, damit das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) als Bundesoberbehörde künftig „schneller agieren“ könne.



















































APOTHEKE ADHOC Debatte