Sicherheits-Server für Apotheken
Die Frist für den „Pillen-Pass“ läuft: Ab 9. Februar 2019 dürfen nur noch verschreibungspflichtige Arzneimittel in den Verkehr gebracht werden, die eine individuelle Seriennummer tragen und die erkennbar unversehrt sind. Die Projektpartner rüsten sich bei Securpharm für den Start: Im kommenden Jahr werden die Apotheken ausgestattet, bereits in den kommenden Monaten geht der Apothekenserver in Betrieb.
In Deutschland wird die Umsetzung der Fälschungsrichtlinie von Securpharm organisiert, einem Zusammenschluss von ABDA, Phagro und den Herstellerverbänden BAH, BPI und VFA. Am Pilotprojekt sind rund 400 Apotheken beteiligt, außerdem sind laut Securpharm-Vorstandssprecher Dr. Reinhard Hoferichter mittlerweile 100 Hersteller an Bord. Er geht davon aus, dass noch einmal so viele Firmen alleine in diesem Jahr dazu kommen.
„Wir sind froh, dass wir mit diesem großen und wichtigen Projekt für den Patientenschutz so früh gestartet sind“, so Hoferichter. Im Laufe des Gemeinschaftsprojektes habe sich gezeigt, dass es mehr Zeit und Aufwand erfordere als ursprünglich angenommen. Der Securpharm-Chef empfiehlt den Firmen, die Prozesse zu trainieren, bevor es ernst wird. „Angesichts der komplexen Anforderungen sind die verbleibenden zwei Jahre für die Umsetzung eine knappe Zeit.“
Auch für Apotheken und Großhandel werde es 2017 spannend. Noch in diesem Jahr soll laut Hoferichter eine neue Version des Apothekenservers fertig gestellt werden, die auf die hohe Nutzeranzahl ausgelegt ist. 2018 schließlich soll die forcierte Nutzeranbindung aller Apotheken und Großhandlungen an das Gesamtsystem erfolgen. „Mit diesem Fahrplan sind wir zuversichtlich, dass wir bis zum 9. Februar 2019 ein funktionierendes technisches System aufbauen, das den Nutzern zur Verfügung steht.“
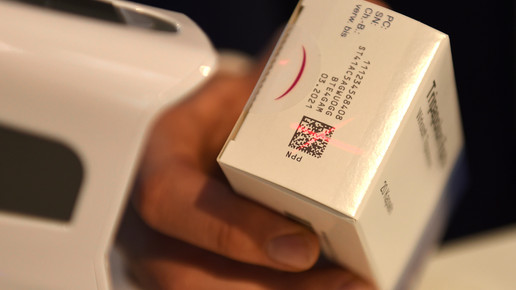
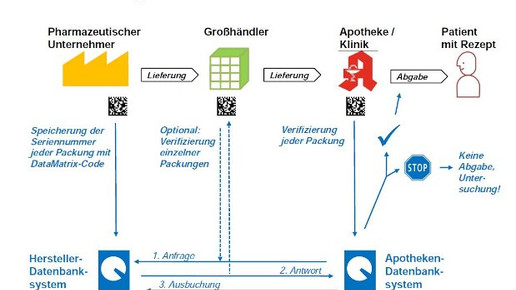
Das Ziel der Fälschungsrichtlinie ist es, dass jede Packung beim Verlassen der Produktion einen individuellen Code erhält und somit identifizierbar wird. Dieser sogenannte „Unique Identifier“ enthält verschiedene Informationen: Produktcode, Seriennummer, gegebenenfalls eine nationale Kennzeichnung, die Chargennummer und das Haltbarkeitsdatum. Im Produktcode sollen der Name des Präparats, die Darreichungsform, die Wirkstärke, die Packungsgröße und die Verpackungsart verschlüsselt sein. Die Seriennummer soll eine maximal 20-stellige Folge aus Zahlen und/oder Buchstaben sein, die zufällig erstellt wird. Die Wahrscheinlichkeit, dass die Nummer abgeleitet werden kann, soll vernachlässigbar gering sein und bei weniger als einem Fall von 10.000 liegen.
Der „Unique Identifier“ wird in einem Data-Matrix-Code auf der Packung verschlüsselt und in nationalen Datenbanken sowie zentral bei einem europäischen Hub hinterlegt. Die Hersteller müssen sicherstellen, dass der spezifische Code, der sich aus Produktcode und Seriennummer ergibt, einmalig bleibt – und zwar für mindestens fünf Jahre oder bis zu einem Jahr nach Ablauf des Haltbarkeitsdatums. Entscheidend ist dabei das spätere Datum.
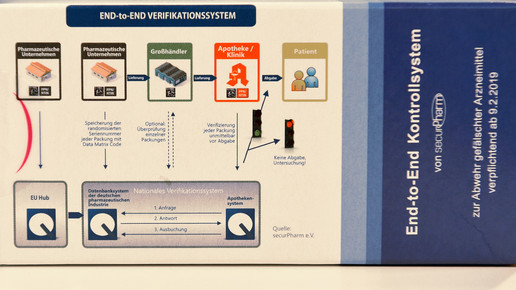
Die Hersteller aktivieren die Codes, bevor sie die Packungen auf den Markt bringen, und melden sie entweder an den europäischen Hub oder nationale oder supranationale Datenbanken. In Deutschland wird diese Datenbank von dem Unternehmen ACS PharmaProtect organisiert, das von BAH, BPI und VFA betrieben wird. Mit der Umsetzung ist der Dienstleister Arvato betraut.
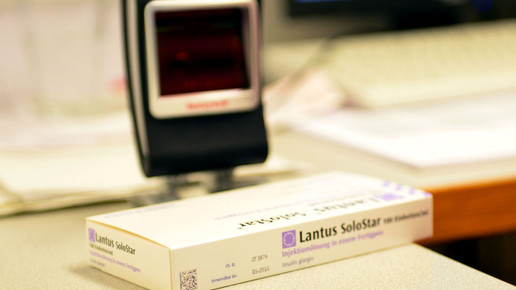
Der Code kann jederzeit eingescannt werden. Auf diese Weise können Großhändler und Apotheker schon beim Wareneingang prüfen, ob die Packungen sicher sind. „Dies hat für Apotheker verschiedene Vorteile, etwa die regelhafte Übernahme von Charge und Verfalldatum in das Warenwirtschaftssystem sowie die klare Zuordnung nicht abgabefähiger Arzneimittel zum jeweiligen Lieferanten“, heißt es bei Securpharm. Großhändler sollen alle Packungen kontrollieren, die von Apotheken retourniert oder von anderen Großhändlern geliefert werden.
Wird ein Arzneimittel an einen Patienten abgegeben, wird der Code eingescannt und die Packung aus dem System abgemeldet. In öffentlichen Apotheken geschieht dies am HV-Tisch. Der Abgleich mit den Datenbanken soll in der Regel innerhalb von 300 Millisekunden erfolgen, so die Vorgabe der EU-Kommission. Es müsse den Apothekern möglich sein, ihre Tätigkeit ohne wesentliche Zeitverzögerungen auszuführen, so Securpharm.
Ist die Nummer in der Datenbank nicht verfügbar oder wurde sie als zurückgerufen oder gestohlen gemeldet, erhält der Apotheker einen entsprechenden Hinweis und gibt diese Information an die zuständigen Behörden weiter.
In Deutschland melden die Apotheken die Abgabe nicht direkt an die nationale Datenbank der Hersteller, sondern an eine zweite Datenbank der ABDA-Tochter Avoxa. So soll sichergestellt werden, dass die Hersteller nicht erfahren, welche Apotheke wann welches Präparat abgegeben hat.
In Krankenhausapotheken können die Arzneimittel zu jedem Zeitpunkt abgemeldet werden – also entweder direkt nach Wareneingang oder kurz vor der Abgabe an den Patienten. Die Mitgliedstaaten können außerdem Ausnahmen für Tierärzte, Zahnärzte, Optiker, Rettungssanitäter, Universitäten, Gefängnisse, Schulen, Hospize oder Pflegeheime festlegen, die direkt von Großhändler beliefert werden. In diesem Fall würden die Lieferanten die Packungen aus dem System abmelden.
Die EU-Verordnung sieht auch einen Plan B vor, falls der automatische Check nicht funktioniert: Apotheken sollen den „Unique Identifier“ in diesem Fall erfassen und später mit der Datenbank abgleichen. Und falls es nur an der Apothekensoftware und nicht am Internet scheitert, sollen Apotheken die Codes auch direkt bei der nationalen Datenbank austragen können.
Die neuen Vorgaben gelten für alle verschreibungspflichtigen Arzneimittel, mit Ausnahme der auf der „White List“ aufgeführten: Das sind derzeit 14 Produktkategorien, darunter etwa Homöopathika, Allergenextrakte, Kontrastmittel und Lösungen für die parenterale Ernährung. OTC-Arzneimittel dürfen die festgelegten Sicherheitsmerkmale nicht tragen. Davon ausgenommen sind Präparate, die auf der „Black List“ stehen und einen Code tragen müssen. Bislang wird dort lediglich Omeprazol aufgeführt – wegen des Fälschungsskandals im Jahr 2013.


































APOTHEKE ADHOC Debatte