Influenza/Covid-19: Kombi-Impfstoff zugelassen
Moderna hat von der Europäischen Kommission die Marktzulassung für den weltweit ersten mRNA-Kombinationsimpfstoff gegen Covid-19 und Influenza erhalten.
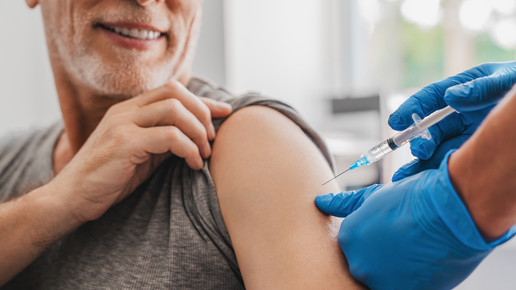
mCombriax (mRNA-1083) ist indiziert zur aktiven Immunisierung zur Vorbeugung einer Influenza-Erkrankung sowie durch SARS-CoV-2 verursachter Covid-19-Erkrankung bei Personen ab 50 Jahren. Die Zulassung gilt innerhalb der Europäischen Union sowie in Island, Liechtenstein und Norwegen.
Die Zulassung stützt sich auf die Ergebnisse einer randomisierten, beobachterverblindeten, aktiv kontrollierten, klinischen Phase-3-Studie zur Bewertung der Sicherheit, Reaktogenität und Immunogenität von mCombriax in zwei unabhängigen Alterskohorten mit jeweils rund 4.000 Erwachsenen. Eine Gruppe mit Erwachsenen ab einem Alter von 65 Jahren verglich den Kombi-Impfstoff mit der gleichzeitigen Gabe vom Hochdosis-Influenzaimpfstoff Fluzone HD (entspricht Efluelda) und Spikevax; Modernas Corona-Impfstoff. Eine weitere Kohorte mit Erwachsenen im Alter von 50 bis 64 Jahren verglich den Kombi-Impfstoff mit der Verabreichung des tetravalenten Grippeimpfstoffes Fluarix (entspricht Influsplit Tetra) in Kombination mit Spikevax.
Alle primären Endpunkte zur Bestätigung der Nicht-Unterlegenheit der Immunantworten wurden erreicht. Nach einer Einzeldosis induzierte mCombriax in beiden Alterskohorten statistisch signifikant höhere Immunantworten gegen drei Influenzavirusstämme (A/H1N1, A/H3N2 und B/Victoria) und gegen SARS-CoV-2. Der B/Yamagata-Stamm, der nicht mehr für die Aufnahme in saisonale Influenza-Impfstoffe empfohlen wird, war der einzige Stamm, für den bei Erwachsenen ab 65 Jahren keine statistisch signifikant höhere Immunantwort im Vergleich zu den gleichzeitig verabreichten zugelassenen Vergleichsimpfstoffen beobachtet wurde.
Die Mehrzahl der erfassten Nebenwirkungen entsprach den bekannten Sicherheitsprofilen der in der Studie verwendeten zugelassenen Impfstoffe.










APOTHEKE ADHOC Debatte