Thema: Risikomeldung/Rückruf
Artikel zum Thema
Rote-Hand-Brief Remsima: Lebensgefährliche Folgen durch Sorbitol
Für Patientinnen und Patienten mit der Erbkrankheit Hereditäre Fruktoseintoleranz (HFI) gibt es einen wichtigen Sicherheitshinweis zur neuen intravenösen Form... Mehr»
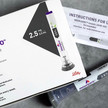
KwikPen modifiziert Keine Restmenge: Neuer Pen für Mounjaro
Bei Mounjaro (Tirzepatid, Lilly) sorgte das Restvolumen, dass nach der vierten Injektion entsorgt werden muss, für Verunsicherungen und Reklamationen bei... Mehr»
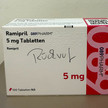
„Wir tauschen um“ Ramipril-Rückruf: So reagieren Apotheken
Ramipril ist ein häufig auf Kassenrezept verordneter Wirkstoff. Der aktuelle Rückruf von 089Pharm sorgt entsprechend für Verunsicherung bei vielen Patientinnen... Mehr»
Diskussionen in Apotheken Ramipril-Rückruf: Hersteller erstattet Ersatzpackung
Nach dem Rückruf von Ramipril von 089Pharm auf Handelsebene hat der Hersteller auf Beschwerden aus Apotheken reagiert. Der Münchener Generikahersteller gewährt... Mehr»
Kritik an fehlender Information Ramipril-Rückruf: Apotheker geht Hersteller an
Die Apotheken und der Großhandel sollen bestimmte Chargen Ramipril 5 mg von 089Pharm zurückschicken. Der Hersteller bedient mit dem ACE-Hemmer mehrere... Mehr»
Probleme bei Bruchfestigkeit 36 Chargen: Nächster Rückruf bei Ramipril
089Pharm hatte bereits im Dezember Ramipril zu 5 mg in verschiedenen Packungsgrößen in zwei Chargen zurückgerufen. Als Grund wurden Abweichungen bei der... Mehr»
Entzugserscheinungen und Autoimmunerkrankung Neue Warnhinweise zu Gabapentin
Die Europäische Arzneimittel-Agentur (EMA) und die nationalen Arzneimittelbehörden der EU-Staaten haben die Sicherheitsinformationen des Antiepileptikums... Mehr»
Migränespritze Anwendungsfehler: Aimovig löst nicht aus
Bei der Arzneimittelkommission (AMK) sind vermehrt Meldungen zu Aimovig (Erenumab, Novartis) eingegangen. Patient:innen berichten einen Defekt des Pens beim... Mehr»
Verdacht auf Cereulid „Beba“ und „Alfamino“: Nestlé ruft Babynahrung zurück
Der Nahrungsmittelkonzern Nestlé ruft mehrere Säuglingsnahrungsprodukte vorsorglich zurück. Hintergrund ist laut Nestlé, dass in einer der Zutaten eines... Mehr»
BfArM-Bescheid Abhängigkeit/Sucht Codein-Tropfen: Zulassung erloschen
1 A Pharma verzichtet auf die Zulassung von Codein 16 mg/ml Tropfen zum Einnehmen. Alle Chargen in Packungen zu 15 und 30 ml wurden zurückgerufen, denn... Mehr»
Medien zum Thema
- 1