Thema: Risikomeldung/Rückruf
Artikel zum Thema
Studienskandal Bupropion: Neuraxpharm droht Lücke
Zulassungsstudien, die nicht den europäischen Standards entsprechen: Seit Dezember hat die Europäische Arzneimittelagentur (EMA) die Zustände beim indischen... Mehr»
AMK-Meldungen Erhöhte Bleiwerte in Antiepileptikum
Blei im Fertigarzneimittel: Desitin vermeldet entsprechende Probleme bei seinem Antikonvulsivum Liskantin. Betapharm muss eine weitere Charge Tilicomp... Mehr»
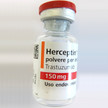
Rote-Hand-Brief Trastuzumab: Herzfunktion überwachen
Mit einem Rote-Hand-Brief weist Roche darauf hin, dass unter Therapie mit Herceptin (Trastuzumab) die Herzfunktion überwacht werden muss. Auch wenn es keine... Mehr»
AMK-Meldungen Betapharm: Blister im falschen Karton
Qualitätsmängel sind auch in dieser Woche die Ursache für Chargenrückrufe. Vor allem Analgetika fallen auf, gleich drei verschiedene Arzneimittel müssen zurück.... Mehr»
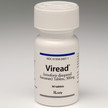
Rote-Hand-Brief Viread: Gefahr der Überdosierung
Gilead meldet in einem Rote-Hand-Brief eine fehlerhafte Angabe der Dosierung in der Packungsinformation zu Viread 204 mg (Tenofovirdisoproxil/TDF). Betroffen... Mehr»
AMK-Meldungen Hersteller ruft feuchte Packungen zurück
Undichte Flaschen, zerbrochene Kapseln: Mehrere Hersteller kämpfen mit Qualitätsmängeln. Die AMK-Meldungen der Woche. Mehr»
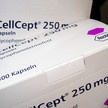
Teratogenität Mycophenolat: Schärfere Sicherheitshinweise
Für den Wirkstoff Mycophenolat, enthalten in CellCept (Roche) und Myfortic (Novartis), gelten neue Hinweise zur Schwangerschaftsverhütung für Frauen und Männer.... Mehr»
Arzneimittelkommission AMK: Neue Profs, gleicher Chef
Der Geschäftsführende Vorstand der ABDA hat den Vorsitzenden und die Mitglieder der Arzneimittelkommission der Deutschen Apotheker (AMK) für die kommenden drei... Mehr»
Rote-Hand-Brief Viridal: Undichte Gummistopfen
Fehler in den Membranstopfen der Alprostadil-Kartuschen des Fertigarzneimittels Viridal veranlassen den Hersteller UCB sein Produkt zurückzurufen. Es bestehe... Mehr»
Medien zum Thema
- 1