FDA will erste rezeptfreie Antibabypille prüfen
Die Antibabypille gehört zu den häufigsten Verhütungsmitteln – dennoch ist der Trend rückläufig, weil immer mehr Frauen auf die Einnahme von Hormonen verzichten wollen. Die US-Arzneimittelbehörde FDA prüft aktuell die Zulassung der ersten rezeptfreien Verhütungspille.
Um die Antibabypille in Deutschland zu erhalten, ist ein Rezept notwendig. Derzeit ist das auch in den USA (noch) der Fall. Doch schon bald könnte dort die erste Verhütungspille freiverkäuflich werden. Frauen könnten sie damit in der Apotheke ohne Rezept erwerben – ähnlich wie Schmerztabletten oder Erkältungsmittel. Die FDA hat für die Überprüfung einen Termin im November angesetzt.
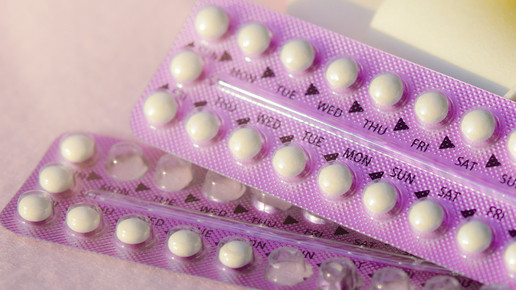
Konkret handelt es sich um die Antibabypille Opill des französischen Herstellers HRA Pharma. Die östrogenfreie Minipille enthält den Wirkstoff Norgestrel aus der Gruppe der Progestine. Er wirkt hemmend auf die Reifung der Eizelle und führt zu einer Viskositätserhöung des Zervixschleims.
HRA Pharma sieht in dem möglichen OTC-Switch eine große Chance: Denn durch die „unnötigen Hürden“ hätten mehr Frauen einen Zugang zu Verhütungsmitteln. Dadurch könnten ungewollte Schwangerschaften verhindert werden. In den USA ist die Zahl besonders hoch.
Debatte um Nebenwirkungen der „Pille“
Doch es gibt immer wieder Diskussionen und Debatten um Nebenwirkungen und mutmaßliche Gefahren hormoneller Kontrazeptiva. Deshalb ist die Zahl der Pillen-Verordnungen in Deutschland seit einigen Jahren rückläufig. Rund jede dritte Anwenderin leidet an Nebenwirkungen, zahlreichen Studien zufolge sind die Pillen der neuen Generationen mit höheren Nebenwirkungsrisiken verbunden, insbesondere einem anderthalb bis zweifach erhöhten Risiko für Thrombosen oder Lungenembolien.
Als besonders hoch gilt das Risiko bei dem Gestagen Drospirenon. So schlägt sich Bayer seit Jahren mit Rechtsstreitigkeiten wegen der erhöhten Thrombosegefahr durch seine Pille Yasminelle herum – gewann jedoch letztlich den Prozess. Kürzlich warnte Pharmakovigilanzausschuss für Risikobewertung (PRAC) der Europäischen Arzneimittel-Agentur (EMA) vor einem erhöhten Meningeom-Risiko unter der Einnahme von Antibabypillen mit hochdosiertem Nomegestrol und Chlormadinon.












APOTHEKE ADHOC Debatte