Klarstellung bei der Meldepflicht nach § 17 Abs. 6a ApBetrO
Seit rund zwei Monaten werden Hämophilie-Präparate wieder in der Apotheke abgegeben. Zum 1. September ist eine entsprechende Änderung des „Gesetzes für mehr Sicherheit in der Arzneimittelversorgung“ (GSAV) in Kraft getreten. Die bisherige Versorgung lief über spezialisierte Hämophilie-Zentren. Mit der Änderung der Abgabe sind auch neue Meldepflichten für die Apotheken in die Apothekenbetriebsordnung aufgenommen worden.
Gemäß § 17 Absatz 6a Apothekenbetriebsordnung (ApBetrO) müssen Apotheken den „Erwerb und [… die] Abgabe von Blutzubereitungen, Sera aus menschlichem Blut und Zubereitungen aus anderen Stoffen menschlicher Herkunft sowie Arzneimitteln zur spezifischen Therapie von Gerinnungsstörungen bei Hämophilie“ dokumentieren und 30 Jahre aufbewahren. Neben der Regelung zur Dokumentation wurde im § 17 Absatz 6a ApBetrO zusätzlich eine neue Meldeverpflichtung ergänzt. Zusätzlich zur Doku muss die Apotheke nach der Abgabe eine Meldung in schriftlicher oder elektronischer Form an den verschreibenden Arzt vornehmen. Diese muss enthalten:
- Arzneimittel- und Chargenbezeichnung sowie Menge
- Abgabedatum
- Name, Vorname, Geburtsdatum und Wohnort des Patienten.
Der Arzt muss die von der Apotheke gemeldeten Daten an das Deutsche Hämophilie-Register (DHR) gemäß § 21 des Transfusionsgesetzes (TFG) weiterleiten. Das DHR sammelt seit 2008 die entsprechenden Daten und wird vom Paul-Ehrlich-Institut geführt.
Im Paragrafen ist festgehalten, dass diese Meldepflicht für folgende Arzneimittelgruppen besteht: Blutzubereitungen, Sera aus menschlichem Blut, Zubereitungen aus anderen Stoffen menschlicher Herkunft und Arzneimitteln zur Behandlung der Hämophilie. Jedoch benötigt lediglich der Verordner von Hämophilie-Produkten die oben genannten Angaben. Bei der Abgabe oder Weiterverarbeitung bei anderen Arzneimitteln wie beispielsweise Humanalbumin oder anderen Blutersatzinfusionen ist die Datenübermittlung überflüssig.
Da sie bisher jedoch gesetzlich festgehalten ist, folgten die Apotheker der ApBetrO und übermittelten die Daten. Nun erfolgt diesbezüglich eine Klarstellung: Die Datenübermittlung ist nur „bei der Abgabe von Arzneimitteln zur spezifischen Therapie von Gerinnungsstörungen bei Hämophilie“ nötig.
Ansonsten werden Hämophilie-Präparate auf einem normalen rosafarbenen Rezept verordnet. Im ersten Schritt – wenn die verordnete Menge als Packungsgröße im Handel ist – ist alles wie bei jedem anderen Muster-16-Rezept; Bestellung und Abgabe des Arzneimittels finden wie gehabt statt und das Rezept wird zulasten der Kasse abgerechnet. Jede Verordnungszeile ist einzeln zu betrachten. Verordnungen sind mit der jeweils verordneten Anzahl von Packungen zu beliefern.
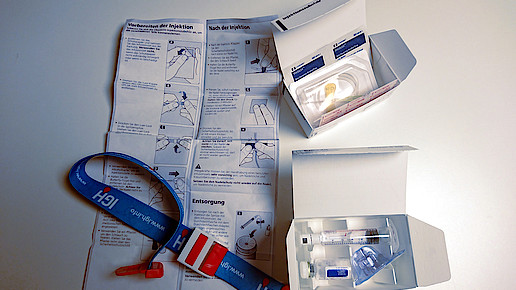
Auch der Patient muss seine Therapie weiterhin dokumentieren. Im sogenannten Substitutionstagebuch sind die Injektionen zu dokumentieren ebenso wie PZN, Chargenbezeichnung, Hersteller, Menge und Stärke sowie Datum und Uhrzeit der Applikation. Diese Dokumentation dient auch der besseren Therapieverfolgung. Es kann gewisse Zeit in Anspruch nehmen, bis ein Patient optimal eingestellt und im Umgang mit den Präparaten geschult ist.
Patienten mit Hämophilie (Bluterkrankheit) fehlen Gerinnungsfaktoren. Unterschieden wird in Hämophilie A – ein Faktor-VIII-Mangel – und Hämophilie B – ein Faktor-IX-Mangel. Hämophilie A tritt dabei häufiger auf. Therapiert wird durch Substitution der fehlenden Gerinnungsfaktoren. Bislang lief die Versorgung der Betroffenen ausschließlich über Hämophilie-Zentren, das bedeutet, die Hersteller haben die Arzneimittel im Direktvertrieb an die spezialisierten Zentren abgegeben.