EMA: Zulassungsantrag für Biontech-Drittimpfung
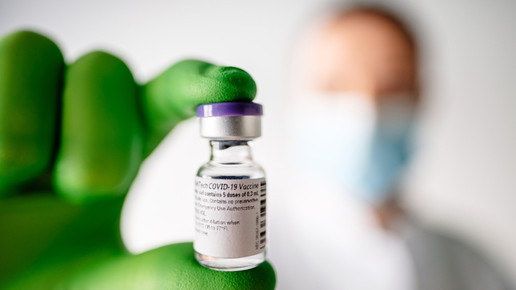
Die Europäische Arzneimittel-Agentur (EMA) hat mit der Evaluierung des Antrages von Biontech zu einer Auffrischimpfung begonnen. Bislang ist Comirnaty als Zwei-Dosis-Schema zugelassen – nun soll die Zulassungserweiterung mittels Drittimpfung für alle ab 16 Jahren erfolgen.
Die EMA untersucht den Nutzen einer Auffrischimpfung mit dem Corona-Impfstoff von Biontech für vollständig geimpfte Menschen ab 16 Jahren. Ergebnisse der Untersuchung, für die Daten des Impfstoffherstellers und laufende klinische Studien ausgewertet werden, sollen in wenigen Wochen vorliegen, teilte die EMA am Montag in Amsterdam mit. In einer zweiten Untersuchung will die EMA zudem prüfen, inwiefern Menschen mit schweren Immunproblemen eine dritte Impfdosis von Biontech oder Moderna hilft. Diese Menschen erzielen durch die ersten beiden Impfdosen möglicherweise keinen ausreichenden Impfschutz.
Wie die EMA bereits in der vergangenen Woche mitgeteilt hatte, sieht sie im Moment keinen drängenden Grund für eine Auffrischimpfung für die gesamte Bevölkerung. Die nun laufenden Untersuchungen sollten eine weiterführende Einschätzung untermauern, hieß es. Wie die EMA betonte, könnten nationale Gesundheitsbehörden sich bereits vorher für eine Auffrischimpfung entscheiden.
Literaturrecherche
Darüber hinaus nutzt die EMA Literaturdaten, um den Nutzen einer dritten Impfdosis besser bewerten zu können. Inwiefern der Impfschutz bei immunsupprimierten Personen abgesenkt sein könnte, ist bisher nicht bekannt. Die Europäische Gesundheitsschutzbehörde ECDC verwies darauf, dass eigentliche Ziel der Impfkampagne – die Vermeidung von schweren und tödlichen Verläufen – nicht aus den Augen zu verlieren. Wie die zugelassenen Booster-Impfstoffe dann tatsächlich eingesetzt werden, hängt auch von den Empfehlungen der nationalen Impfkommissionen ab.





















APOTHEKE ADHOC Debatte