Securpharm kommt später
Zum Schutz vor Arzneimittelfälschungen sollen Arzneimittel künftig mit einem individuellen Data-Matrix-Code versehen werden. In den Apotheken soll so vor der Abgabe garantiert werden können, dass es sich um Originalware handelt. Ursprünglich sollten die Vorgaben ab 2017 gelten. Doch jetzt kommt die EU-Fälschungsrichtlinie voraussichtlich erst 2019.
Die EU-Kommission arbeitet noch an dem delegierten Rechtsakt, mit dem die Vorgaben der Fälschungsrichtlinie umgesetzt werden. Die Verordnung soll im September präsentiert und im ersten Quartal 2016 veröffentlicht werden. Entsprechend könnte die Richtlinie später als geplant erst Anfang 2019 in Kraft treten.
Auf europäischer Ebene arbeiten die Pharmaverbände EFPIA und EGA, der Verband der Reimporteure EAEPC sowie der Großhandelsverband GIRP und der Apothekerverband PGEU in der European Medicines Verification Organisation (EMVO) zusammen. Als Vorsitzende hat Sonia Ruiz, Vertreterin des spanischen Apothekerverbandes in Brüssel, den ehemaligen PGEU-Generalsekretär John Chave beerbt.
Während für die Umsetzung die Mitgliedstaaten verantwortlich sind, leistet EMVO gerade auf organisatorischer und technischer Ebene wichtige Vorarbeit. So wurden vor kurzem Rahmenverträge mit den Dienstleistern Arvato, Aegate und Solidsoft Reply geschlossen, die die Arbeitsgruppen in den Mitgliedstaaten dann beauftragen können.
Arvato gehört zu Bertelsmann und ist bei Securpharm bereits mit der Umsetzung betraut. Solidsoft hat das europäische Hub für EMVO entwickelt; das britische Unternehmen wurde 1993 als Entwickler für Microsoft-Anwendungen gegründet und gehört seit Ende 2013 zur börsennotierten Reply-Gruppe aus Italien. Aegate kommt ebenfalls aus Großbritannien und hat in den vergangenen sieben Jahren Erfahrungen mit der Verifizierung von Arzneimitteln gesammelt. Hinter der Firma steht ein Finanzinvestor.
Die Regelung gilt für alle verschreibungspflichtigen Arzneimittel. Ausgenommen davon sind Präparate, für die kein Fälschungsrisiko festgestellt wurde und die auf einer „White list“ geführt werden. Andersherum müssen OTC-Präparate keine Sicherheitsmerkmale tragen, außer für sie wurde ein Fälschungsrisiko festgestellt und sie stehen auf einer „Black list“. Omeprazol ist so ein Beispiel, das seit dem Fälschungsskandal als unsicher eingestuft wird – auch wenn damals die verschreibungspflichtige Variante betroffen war.
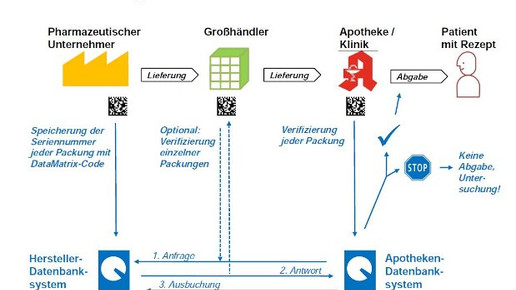
In Deutschland werden die neuen Vorgaben mit dem Projekt Securpharm bereits erprobt. Beteiligt sind die Apotheken über die ABDA, die Großhändler über den Phagro und die Industrie über BAH, BPI, Pro Generika und den VFA. Die Unternehmen generieren dafür Seriennummern, die in einer nationalen Datenbank gesammelt werden.
Das Unternehmen ACS PharmaProtect, das von den Herstellerverbänden BAH, BPI und VFA betrieben wird, organisiert die Daten. Parallel dazu werden die Informationen an die ABDA-Tochter Werbe- und Vertriebsgesellschaft Deutscher Apotheker (WuV) übermittelt. Scannt ein Apotheker ein Arzneimittel mit einem Securpharm-Code ein, erfährt er unmittelbar danach, ob die Seriennummer bekannt ist oder nicht.
























APOTHEKE ADHOC Debatte