Schwere Hautreaktion: Ibuprofen/Pseudoephedrin bekommt Warnhinweis
Die Kombination aus Ibuprofen und Pseudoephedrin ist bei Verbrauchern in der Erkältungszeit beliebt. Kritiker warnen seit Langem vor dem Gebrauch von Kombi-Präparaten bei grippalen Infekten. Im Rahmen eines Risikobewertungsverfahrens sollen Arzneimittel mit der Kombination Ibuprofen/Pseduoephedrin Änderungen der Fach- und Gebrauchsinformationen erfahren, nur so könne das Nutzen-Risiko-Profil weiterhin als positiv eingestuft werden.
Basierend auf der Empfehlung des Ausschusses für Risikobewertung im Bereich der Pharmakovigilanz (PRAC) der Europäischen Arzneimittelbehörde (EMA) hat die Koordinierungsgruppe (CMDh) einen einstimmigen Beschluss gefasst. Grundlage sind Literaturdaten, die einen kausalen Zusammenhang zwischen der Anwendung der Wirkstoffkombination und dem Auftreten schwerer Hautreaktionen wie beispielsweise einer akuten generalisierten exanthematischen Pustulose (AGEP) nicht ausschließen können. Mit Bescheid vom 15. Oktober setzt das Bundesinstitut für Arzneimittel und Risikobewertung (BfArM) den Beschluss der Koordinierungsgruppe um.
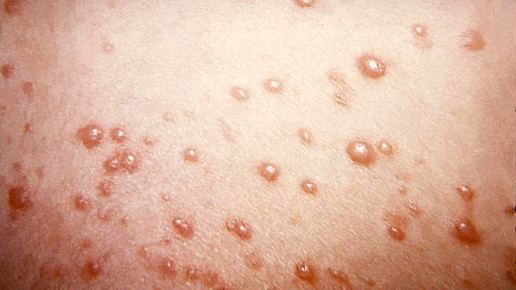
Entsprechende Präparate sollen künftig innerhalb der EU folgende Angaben in der Fach- und Gebrauchsinformation enthalten. Abschnitt 4.4 soll um folgenden Warnhinweis ergänzt werden: „Schwere Hautreaktionen wie AGEP können bei Pseudoephedrin-haltigen Arzneimitteln auftreten.“ Der Ausschlag könne bereits an den ersten beiden Behandlungstagen auftreten und von Fieber sowie zahlreichen, kleinen, hauptsächlich nicht-follikulären Pusteln begleitet sein. Das Erythem kann hauptsächlich in den Hautfalten, am Rumpf und an den oberen Extremitäten auftreten.
„Die Patienten sollten sorgfältig überwacht werden. Wenn Anzeichen und Symptome wie Fieber, Erythem oder viele kleine Pusteln beobachtet werden, sollte die Anwendung des Arzneimittels beendet und erforderlichenfalls geeignete Maßnahme ergriffen werden.“ Eine Änderung soll es auch in Abschnitt 4.8 bezüglich der unerwünschten Arzneimittelwirkungen geben. Unter dem Punkt „Erkrankungen der Haut und des Unterhautzellgewebes“ soll mit einer „nicht bekannten“ Häufigkeit der Hinweis: „Schwere Hautreaktionen, einschließlich AGEP“ aufgenommen werden.
In der Packungsbeilage wird in Abschnitt 2 „Warnhinweise und Vorsichtsmaßnahmen“ folgender Hinweis aufgenommen: „Wenn Sie eine fiebrige generalisierte Hautrötung verbunden mit Pusteln bekommen, beenden Sie die Einnahme des Arzneimittels und wenden Sie sich unverzüglich an einen Arzt.“ Entsprechend ist Abschnitt 4 um die dazugehörigen Symptome zu ergänzen.
Hierzulande enthalten beispielsweise Boxagrippal (Sanofi), SpaltGrippal (Pfizer), DuoGrippal (Procter & Gamble (P&G)) sowie die Generika von Hexal und Ratiopharm die Wirkstoffkombination. Ibuprofen wirkt schmerzlindernd, entzündungshemmend und fiebersenkend. Der Wirkstoff hemmt nicht-selektiv die Cyclooxigenasen I und II (COX-1 und -2) und vermindert somit die Produktion von Prostaglandinen, die Entzündungen vermitteln. Besonders die Prostaglandine, die aus der Arachidonsäure-Kaskade entstehen, verstärken Entzündungen und die Schmerzwahrnehmung. Die Halbwertszeit beträgt etwa zwei bis drei Stunden. Zu den häufigsten Nebenwirkungen zählen gastrointestinale Beschwerden.
Pseudoephedrin ist ein indirektes Sympathomimetikum und wirkt stimulierend. Der Wirkstoff schüttet verstärkt Catecholamine aus und hemmt deren Wiederaufnahme. Die Folge ist eine Gefäßverengung und eine abschwellende Wirkung auf die Nasenschleimhäute. Das „Nasenspray zum Einnehmen“ hat eine Halbwertszeit von etwa 9 bis 16 Stunden. Nebenwirkungen können Herzrasen, Blutdruckanstieg oder Unruhe sein.
















APOTHEKE ADHOC Debatte