Avastin-Biosimilar erhält EU-Zulassung
Erstes Bevacizumab-Biosimilar zugelassen: Mvasi (Amgen/Allergan) kann zur Behandlung verschiedener Krebsarten eingesetzt werden. Möglich sind auch Kombinationen mit anderen Onkologika.
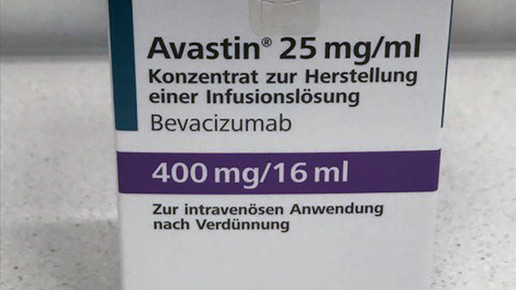
Mvasi hat die Zulassung für verschiedene Krebsarten erhalten. Grundlage sind Daten, die keine bedeutenden Abweichungen zwischen Referenzarzneimittel und Biosimilar in puncto Sicherheit, Wirksamkeit und Qualität belegen. Das Biosimilar zu Avastin (Roche) kann beispielsweise zur Behandlung von Dickdarm- oder Enddarmkarzinomen, Brustkrebs, nicht-kleinzelligem Lungenkrebs, Nierenzellkarzinom, epithelialem Eierstock-, Eileiter- oder primärem Peritonealkarzinom und Tumoren des Gebärmutterhalses eingesetzt werden.
Bevacizumab kommt zusätzlich zu einer platinhaltigen Chemotherapie als First-Line-Therapie zur Behandlung von Erwachsenen mit inoperablem fortgeschrittenem, metastasiertem oder rezidivierendem nicht-kleinzelligem Bronchialkarzinom (NSCLC) zum Einsatz, ausgenommen sind Patienten mit vorwiegender Plattenepithel-Histologie. In Kombination mit Erlotinib ist das Arzneimittel zur First-Line-Behandlung von Erwachsenen mit inoperablem fortgeschrittenem, metastasiertem oder rezidivierendem nicht-kleinzelligem Nicht-Plattenepithel-Bronchialkarzinom mit Mutationen, die den epidermalen Wachstumsfaktorrezeptor (EGFR) aktivieren, indidziert.
Möglich sind außerdem Therapien in Kombination mit Interferon alfa-2a bei fortgeschrittenem und/oder metastasiertem Nierenzellkarzinom, in Kombination mit Carboplatin und Paclitaxel, Carboplatin und Gemcitabin und Paclitaxel, Topotecan oder pegyliertem liposomalem Doxorubicin bei Platin-sensitivem oder Platin-resistentem rezidiviertem epithelialem Ovarial-, Eileiter- oder primärem Peritonealkarzinom und in Kombination mit Paclitaxel und Cisplatin oder alternativ Paclitaxel und Topotecan bei persistierendem, rezidiviertem oder metastasiertem Zervixkarzinom.
In Kombination mit einer Fluoropyrimidin-basierten Chemotherapie kann Mvasi auch für die Behandlung von Erwachsenen mit metastasierendem Kolon- oder Rektumkarzinom angewendet werden. In Kombination mit Paclitaxel ist das Biosimilar für die First-Line-Behandlung von Erwachsenen mit metastasierendem Mammakarzinom indiziert. In Kombination mit Capecitabin könnte der monoklonale Antikörper zur First-Line-Behandlung von erwachsenen Patienten mit metastasiertem Brustkrebs angewendet werden, wenn eine Behandlung mit anderen Chemotherapie-Optionen, einschließlich Taxanen oder Anthracyclinen, als nicht geeignet angesehen wird.
Der monoklonaler Antikörper bindet an den vaskulären endothelialen Wachstumsfaktor (VEGF). Dieser gilt als Schlüsselfaktor der Vaskulogenese und Angiogenese. Die Bindung von VEGF an seine Rezeptoren auf der Oberfläche des Endothels wird gehemmt. Die Neutralisierung der biologischen Aktivität von VEGF reduziert die Vaskularisierung von Tumoren, normalisiert das vorhandene Tumorgefäßsystem und inhibiert die Bildung neuer Tumorgefäßsysteme, wodurch das Tumorwachstum gehemmt wird. Der Angiogenesehemmer verhindert somit maßgeblich die Bildung neuer Blutgefäße, die den Tumor versorgen sollen.
Die Zulassung erlaubt Amgen und Allergan, Mvasi in den 28 EU-Mitgliedsstaaten sowie Norwegen, Island und Lichtenstein zu vertreiben. Im September 2017 hatte das Arzneimittel die Zulassung in den USA erhalten. Amgen und Allergan arbeiten bei der Entwicklung und Vermarktung von vier Onkologie-Biosimilars zusammen.













APOTHEKE ADHOC Debatte