Kayshild: Semaglutid gegen Fettleber
Novo Nordisk hat die Zulassung für Kayshild erhalten. Somit kann der Wirkstoff Semaglutid auch bei Fettlebererkrankungen eingesetzt werden.
Ab sofort gibt es eine neue Option bei einer Fettlebererkrankung. Der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Arzneimittel-Agentur (EMA) hatte die bedingte Zulassung von Kayshild (Novo Nordisk) im Februar empfohlen. Die EU-Kommission hat die Zulassung nun erteilt.
Erstes GLP-1 gegen Fettleber
Somit kann Semaglutid, das bereits für Ozempic (Diabetes) und Wegovy (Adipositas) etabliert ist, als der erste GLP-1-Rezeptoragonist zur gezielten Therapie der metabolisch-assoziierter Steatohepatitis (MASH) bei Erwachsenen eingesetzt werden.
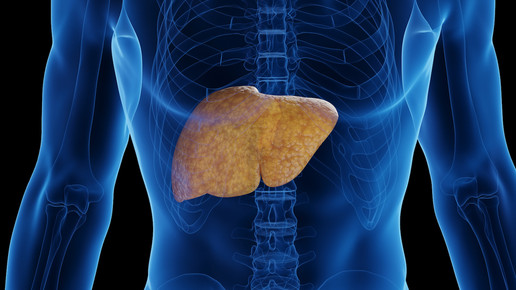
Bei MASH führen Fettablagerungen zu Entzündungen und Zellschäden im Lebergewebe. Die Erkrankung gilt als schwere Form der nichtalkoholischen Fettlebererkrankung. Kayshild ist für Patientinnen und Patienten vorgesehen, deren Leber bereits mäßige bis fortgeschrittene Vernarbungen (Fibrosestadien F2 bis F3) aufweist. Ein irreversibles Organversagen, also eine Zirrhose, liegt in diesem Stadium noch nicht vor. Die Behandlung soll ergänzend zu Diät und Bewegung erfolgen.
Auflösung von MASH
Semaglutid wirkt indirekt auf die Leber, indem es Stoffwechselfaktoren wie Körpergewicht, Glukose- und Fettstoffwechsel verbessert sowie Entzündungen und Fetteinlagerungen reduziert. In Studien erzielte das Präparat signifikante Erfolge bei der Auflösung der MASH und der Verbesserung der Fibrose.
Kayshild wird als Injektionslösung in Fertigpens in Stärken von 0,25 mg bis 2,4 mg verfügbar sein. Als häufigste Nebenwirkungen können gastrointestinale Beschwerden und Müdigkeit auftreten.
Neben dem oral verfügbaren Wirkstoff Resmetirom (Rezdiffra) ist Kayshild der zweite in der EU zugelassene Wirkstoff gegen die Fettlebererkrankung.











APOTHEKE ADHOC Debatte