Cablivi schützt vor Mikrothromben
Nanobody gegen erworbene thrombotische thrombozytopenische Purpura (aTTP): Mit Cablivi (Caplacizumab, Sanofi) ist seit Oktober die erste spezifische Therapie der aTTP – eine seltene lebensbedrohliche Erkrankung – verfügbar.
Die aTTP ist eine immunvermittelte Blutgerinnungsstörung, an der drei bis sieben Patienten auf eine Million Menschen erkranken. Die seltene Erkrankung tritt akut auf und ist von lebensbedrohlichen Episoden gekennzeichnet, die für bis zu 20 Prozent der Betroffenen tödlich enden. Die Standardtherapie bestand bislang aus Immunsuppression und Plasmatransplantation. Cablivi hat Ende August die EU-Zulassung als Ergänzung zur Standardtherapie bei Erwachsenen mit einer aTTP-Episode erhalten.
Der humanisierte bivalente Nanokörper hemmt die Interaktion von Thrombozyten und von-Willebrand-Faktor (vWF). Caplacizumab unterbindet sogenannte Mikrothromben, das sind durch von-Willebrand-Faktor vermittelte Plättchenadhäsionen, die für die aTTP charakteristisch ist. Der Arzneistoff vermag die Zahl der Thrombozyten, die Rezidivrate oder auch die Dauer von Krankenhausaufenthalten zu reduzieren. Gleichzeitig werden der Faktor-VIII-Spiegel reduziert und der Gesamt-vWF-Antigenspiegel verringert.
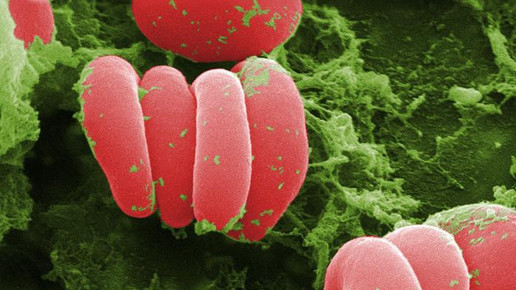
Die Bildung der Mikrothromben – eine unkontrollierte Bindung von Thrombozyten an ultralange vWF-Multimere (ULvWF) – kann auf eine Autoimmunreaktion gegen das Enzym ADAMTS13 zurückgeführt werden, die deren Spaltung verhindert. Cablivi unterbindet die Interaktion zwischen ULvWF und Thrombozyten, die Bildung der Mikrothromben bleibt aus.
Die starke Gerinnselbildung erfolgt bei einer aTTP vor allem in den kleinen Blutgefäßen. Die Folge sind eine schwere Thrombozytopenie oder ein Verlust von roten Blutkörperchen. Die blutplättchenreichen Gerinnsel können zu schwerwiegenden Organschäden führen. Betroffen sind vor allem Herz, Gehirn und Niere.
Der Nanobody wird als intravenöse Injektion zu 10 mg Caplacizumab vor der Plasmapherese verabreicht. Zu den häufigsten unerwünschten Arzneimittelwirkung unter Cablivi zählen Blutungen. Aber auch Pyrexie, Müdigkeit, Kopfschmerzen, Myalgie oder Reaktionen wie Erythem und Juckreiz an der Einstichstelle wurden beobachtet.
Caplacizumab ist der erste Nanobody aus dem Hause Sanofi und wurde von Ablynx entwickelt. Die Zulassung basiert auf Daten der Phase-III-Studie Hercules mit 145 Probanden – 72 wurden mit Caplacizumab, 73 mit Placebo behandelt. Die Studie belegt Sicherheit und Wirksamkeit bei einer Anwendung zusätzlich zur Standardbehandlung. Eine Behandlung mit Caplacizumab zusätzlich zur Standardtherapie führte gegenüber Placebo zu folgenden Ergebnissen:
- 55 Prozent höhere Wahrscheinlichkeit für ein Ansprechen der Thrombozytenzahl
- 74 Prozent weniger Patienten mit aTTP-bedingten Todesfall, aTTP-Exazerbationen, oder einem schwerwiegenden thromboembolischen Ereignis während des Behandlungszeitraums
- 67 Prozent weniger Rezidive während des gesamten Studienzeitraums.










APOTHEKE ADHOC Debatte