Ramipril-Rückruf: Apotheker geht Hersteller an
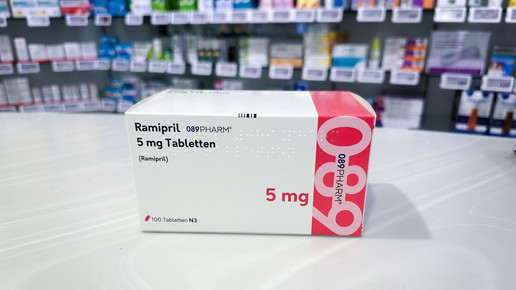
Die Apotheken und der Großhandel sollen bestimmte Chargen Ramipril 5 mg von 089Pharm zurückschicken. Der Hersteller bedient mit dem ACE-Hemmer mehrere Rabattverträge. Die Nachricht sorgt auch für Verunsicherung bei der Kundschaft. Mehrere Apotheken berichten von Diskussionen im HV. Ein Inhaber aus Hessen fordert vom Hersteller eine Stellungnahme.
Der Ramipril-Rückruf – Ramipril 089PHARM 5 mg zu 20, 50 und 100 Tabletten – erfolgt auf Handelsebene, das heißt Großhandel und Apotheken sind betroffen. Als Grund nennt der Münchener Hersteller Beanstandungen zur Bruchfestigkeit der Tabletten. Es handelt sich um im Markt befindliche Chargen mit einer Haltbarkeit bis einschließlich Juni 2027. Chargen mit späterem Verfall – ab Oktober 2027 – sind laut Hersteller nicht betroffen, weil die Spezifikationen für die Bruchfestigkeit bereits angepasst wurde.
Die Bruchfestigkeit beeinflusst unter anderem die Zerfallszeit und die Freisetzungsgeschwindigkeit des Wirkstoffes. Einfluss auf die Bruchfestigkeit von Tabletten hat unter anderem der Pressdruck. Zuvor gab es bereits einen Ramipril-Rückruf des Herstellers.
Apotheken werden gebeten, das Warenlager zu überprüfen und betroffene Packungen zurückzuschicken. Retouren werden zu 100 Prozent vergütet. Inhaber Andreas Grünebaum von der Easy-Apotheke Bruchköbel ist die Information zu wenig. Denn allein von Freitagnachmittag bis Samstag seien bereits fünf verunsicherte Kundinnen und Kunden wegen des Rückrufs beraten worden, obwohl dieser eben nicht auf Patientenebene ausgesprochen wurde. „Dies entspricht etwa 5 bis 6 Prozent der seit November abgegebenen Packungen von Ramipril 089Pharma 5mg“, sagt er. Noch seien Alternativen des Präparats lieferbar. „Wir haben in den vergangenen zehn Wochen eine dreistellige Anzahl von Packungen dieser Firma abgegeben, von denen bereits innerhalb von zwei Tagen sechs von Kunden zurück in die Apotheke gebracht wurden.“
Neben der Verunsicherung der Kundschaft gebe es auch Konsequenzen für Apotheken und Arztpraxen. „Wir haben einen Mehraufwand aufgrund der Beratung der verunsicherten Patienten.“ Verordnerinnen und Verordner müssten gegebenfalls eine eigentlich in der Regel in diesem Fall unnötige Ersatzverordnung ausstellen.
Keine Probleme bei Apothekenkundschaft
Die Kundschaft selbst meldete ihm zufolge keine Probleme bei der Einnahme wegen brüchigen oder gar zerbröselnden Tabletten. In der Apotheke sei das Team jedoch verunsichert, ob man ohne Weiteres einfach eine andere Packung im Austausch abgeben könne oder dürfe.
Der Apotheker fordert vom Hersteller eine Klarstellung, ob auszuschließen sei, dass für Patientinnen oder Patienten „konkrete Gefahren oder Nachteile bei der Einnahme aus den beanstandeten Chargen entstehen“. Zudem kritisiert er die fehlende Information bezüglich der Erstattung von bereits benutzten Präparaten. „Werden auch angebrochene Packungen nach „‚Ersatzverordnung gemäß § 31 Absatz 3 Satz 7 SGB V‘ von Ihnen zu 100 Prozent erstattet“, fragt er.
Grünebaum wünscht sich vom Hersteller eine Information über mögliche Gefahren oder Auswirkungen in schriftlicher Form, die er seinen Kundinnen und Kunden vorlegen kann.
Ersatzverordnung
Die Ersatzverordnung ist in § 31 Abs. 3 Satz 7 Sozialgesetzbuch (SGB V) geregelt. Demnach haben Versicherte Anspruch auf ein Ersatzpräparat, wenn für ein Arzneimittel auf Grund eines Arzneimittelrückrufs oder einer von der zuständigen Behörde bekannt gemachten Einschränkung der Verwendbarkeit erneut ein Arzneimittel verordnet werden muss. Darf das zurückgerufene Arzneimittel nicht mehr eingenommen werden, ist die erneute Verordnung zuzahlungsfrei. Da der aktuelle Ramipril-Rückruf nicht auf Patientenebene erfolgt, kommt die Ersatzverodnung nicht zum Tragenn.
Ersatzverordnungen können sowohl auf Muster 16 als auch als E-Rezept ausgestellt werden. Bei der Kennzeichnung und Bedruckung gibt es jedoch einige Unterschiede zu beachten.
Ersatzverordnung auf Muster 16
- Ersatzverordnung gemäß § 31 Absatz 3 Satz 7 SGB V muss angegeben sein
- 1. Zeile: Sonderkennzeichen 06461067, Faktor 1, Taxe 0
- 2. Zeile: PZN Ersatzarzneimittels, Faktor entspricht der Anzahl abgegebener Packungen, Apothekenverkaufspreis (AVP)
- wenn Zuzahlungsstatus von Praxis nicht richtig gekennzeichnet: gebührenbefreit ankreuzen und abzeichnen
Ersatzverordnung auf E-Rezept
- Kennzeichnung in der Apothekensoftware angezeigt
- Zusatzattribut Gruppe 8 (Ersatzverordnung), Schlüssel 1 ja
- wenn von Praxis nicht richtig gekennzeichnet: Zusatzattribut Gruppe 15 (von Zuzahlungspflicht befreit), Schlüssel 1 ja
Hersteller gehört zu Polpharma
Von 089Pharm war bislang keine Stellungnahme zu erhalten. Der Hersteller bedient nach eigenen Angaben mit Ramipril mehrere Rabattverträge der 5 mg und 10 mg Tabletten jeweils im „Drei-Partner-Modell“. Seit Anfang Januar mit SpektrumK; seit November 2025 mit der Knappschaft und seit Juli 2025 mit Ersatzkassen/vdek. Insgesamt bedient das Unternehmen elf Rabattverträge.
Der Generikaanbieter gehört zu Polpharma, einer der führenden Hersteller aus Polen. Schon vor zehn Jahren hatte der Konzern gemeinsam mit den Strüngmann-Brüdern einen ersten Anlauf unternommen, um im deutschen Markt Fuß zu fassen. Mittlerweile ist das Joint Venture Bioeq in Formycon aufgegangen. Polpharma wurde 1935 gegründet und im Juli 2000 privatisiert; damals übernahmen ein Konsortium um die Investoren Spectra und Prokom den Hersteller. Die Holding befindet sich heute in Amsterdam, diese wiederum gehört zu einer Investmentfirma mit Sitz auf Zypern.
lesen Sie weiter.