Zulassungserweiterung: Kerendia bei Herzinsuffizienz
Von Herzinsuffizienz sind weltweit über 64 Millionen Menschen betroffen, davon mindestens 15 Millionen allein in Europa. Mit Finerenon wurde nun ein Wirkstoff zugelassen, mit dem eine linksventrikuläre Auswurfleistung von mindestens 40 Prozent bei Erwachsenen behandeln werden kann.
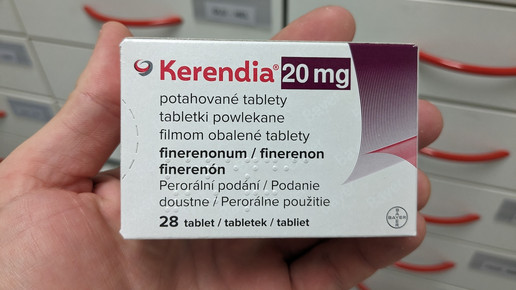
Unter dem Handelsnamen Kerendia (Bayer) wurde in der EU der Wirkstoff Finerenon für die Behandlung von Erwachsenen mit chronischer Herzinsuffizienz zugelassen, deren linksventrikuläre Auswurfleistung (LVEF) bei 40 Prozent oder höher liegt. Dadurch erweitert sich das Einsatzgebiet des Medikaments, das bisher primär für Patient:innen mit chronischer Nierenerkrankung und Typ-2-Diabetes eingesetzt werden kann.
Kerendia schließt Lücke
Die Zulassung im Bereich Herzinsuffizienz schließt laut Bayer eine kritische Lücke in der Versorgung von Millionen von Menschen. „Patienten mit Herzinsuffizienz und einer linksventrikulären Auswurfleistung von 40 Prozent oder höher stellen eine große und wachsende Patientengruppe mit schlechter Prognose dar, die erheblichen klinischen Herausforderungen wie wiederholten Krankenhausaufenthalten aufgrund der Verschlechterung der Herzinsuffizienz sowie einem hohen Sterblichkeitsrisiko ausgesetzt sind“, erklärt Professor Dr. Scott D. Solomon, Direktor des Clinical Trials Outcomes Centers der Harvard Medical School und Vorsitzender des Executive Committee der Studie.
Finerenon adressiere die Überaktivierung des Mineralokortikoid-Rezeptors, einem wesentlichen pathophysiologischen Treiber bei Herzinsuffizienz. Basierend auf seiner nachgewiesenen Wirksamkeit in der Finearts-HF-Studie könne Kerendia zu einer neuen Säule der umfassenden Versorgung werden, um die Prognose dieser vulnerablen Patientenpopulation mit hohem ungedeckten medizinischen Bedarf zu verbessern, so der Experte weiter.
Studie mit 20.000 Patienten
Kerendia habe seine Wirksamkeit bei der Reduktion des kombinierten Risikos aus Herzinsuffizienz-Ereignissen und kardiovaskulärem Tod unabhängig von der Begleittherapie und klinischem Setting nachgewiesen. „Die robuste Datenlage aus fünf Phase-III-Studien, die über 20.000 Patienten aus verschiedenen Patientengruppen mit chronischer Nierenerkrankung und/oder Herzinsuffizienz umfassen, unterstreicht das Potenzial von Kerendia, zu einer grundlegenden Therapiesäule sowohl für Herzinsuffizienz mit LVEF 40 Prozent oder höher als auch für chronische Nierenerkrankung zu werden“, so Bayer.
Herzinsuffizeinz als wachsendes Problem
Herzinsuffizienz stellt ein schnell wachsendes Problem der öffentlichen Gesundheit dar. Etwa die Hälfte der betroffenen Patient:innen leidet an Herzinsuffizienz mit einer linksventrikulären Auswurfleistung (LVEF) von ≥ 40 Prozent. Diese Form ist häufig mit mehreren Komorbiditäten wie chronischer Nierenerkrankung, Bluthochdruck und Vorhofflimmern verbunden. In Folge kommt es zu Hospitalisierungen und einer erhöhten Sterblichkeit. Die durch Herzinsuffizienz entstehenden Kosten in der EU werden mittlerweile auf jährlich 29 Milliarden Euro geschätzt.
Das Problem: Aktuell stehen nur wenige zugelassene und leitliniengerechte Therapieoptionen zur Verfügung. Gleichzeitig sind die Betroffenen einem hohen Risiko für kardiovaskuläre Ereignisse ausgesetzt. Prognosen deuten darauf hin, dass diese wachsende Patientengruppe schon in naher Zukunft den Großteil der aufgrund von Herzinsuffizienz stationär behandelten Patienten ausmachen wird.













APOTHEKE ADHOC Debatte