Biosimilar-Austausch: Viele Fallen für Apotheken
Ab heute gelten für biotechnologisch hergestellte Arzneimittel dieselben Austauschregeln wie für andere Arzneimittel. Eine Stolperfalle ist das Device. Denn ein Austausch ist möglich, wenn die Biologika eine gleiche oder eine austauschbare Darreichungsform besitzen, es muss aber auch das Behältnis übereinstimmen. Doch auch zwischen den identischen Devices gibt es Unterschiede – beispielsweise ist Pen nicht gleich Pen.
Zum 1. April sind die Änderungen des Rahmenvertrages in Kraft getreten. Dazu gehören auch die Austauschregeln bei biotechnologisch hergestellten Arzneimitteln. Beim Austausch sind die Vorgaben in § 40c Arzneimittel-Richtlinie (AM-RL) zu beachten. Darin ist festgelegt, dass Apotheken bei der Abgabe von Biologika zur Abgabe preisgünstiger Arzneimittel verpflichtet sind.
- Liegt ein Rabattvertrag vor, muss dieser bedient werden.
- Liegt kein Rabattvertrag vor, ist eines der vier preisgünstigeren Präparate abzugeben.
- Für den Austausch gilt:
- Das abzugebende Produkt ist für mindestens ein gleiches Anwendungsgebiet sowie mindestens für dieselbe Applikationsart zugelassen wie das verordnete.
- Das abzugebende und das verordnete Arzneimittel müssen in Wirkstärke und Packungsgröße identisch sein und die gleiche oder eine austauschbare Darreichungsform haben.
- Beide Präparate haben die gleiche Darreichungsform, auch das Behältnis – wie beispielsweise Fertigspritze, Fertigpen oder Patrone – muss identisch sein.
Hat die verschreibende Person einen Austausch aus medizinisch-therapeutischen Gründen ausgeschlossen, muss die Apotheke auch nicht austauschen.
Welche Präparate aut-idem-konform ausgetauscht werden können und müssen, wurde von der Abdata in die Apothekensoftware eingespielt.
Unübersichtlicher Markt
Am Beispiel Humira (Adalimumab) 40 mg/0,4 ml zeigt sich die Komplexität. Das Arzneimittel ist als Injektionslösung in einer Fertigspritze und als Fertigpen im Handel. Für die Injektionslösung in einer Fertigspritze gibt es 128 Artikel, die als aut-idem-konform nach Rahmenvertrag gelten. Bei der AOK Nordost gibt es 31 Rabattverträge. Beim Fertigpen gelten 60 Artikel als aut-idem-konform und bei 44 Präparaten sind die Anbieter den Open-House-Verträgen beigetreten.
Folgende Präparate sind derzeit auf dem Markt:
- Humira (AbbVie)
- Amgevita (Amgen)
- Amsparity (Pfizer)
- Hyrimoz (Hexal/Sandoz)
- Hukyndra (Stada)
- Hulio (Viatris/Mylan)
- Idacio (Fresenius Kabi)
- Imraldi (Biogen)
- Yuflyma (Celltrion)
Zusätzlich gibt es zu jedem Präparate eine ganze Reihe von Parallelimporten. Je nach Hersteller unterscheiden sich die Wirkstärken und Packungsgrößen, teilweise gibt es bestimmte Varianten nur als Import: Bei Humira etwa ist die Dosierung à 80 mg/0,8 ml als Original nur als Pen erhältlich, als Import gibt es aber auch Fertigspritzen. Auch die Dosierung à 40 mg/0,8 ml wird von Humira und Hyrimoz nur als Import angeboten – und zwar nur als Spritze. Bei Imraldi gibt es hier auch einen Pen als Import.
Eine Übersicht mit den unterschiedlichen Präparaten und Anbietern gibt es hier als Download.
Risiko: Device
Liegt in der Apotheke eine Verordnung über die Injektionslösung in einer Fertigspritze vor, aber der/die Versicherte wurde bislang mit dem Fertigpen behandelt, kann die Apotheken nicht austauschen, da die Präparate zwar für das gleiche Anwendungsgebiet und die gleiche Applikationsart zugelassen sind und auch die Darreichungsform identisch ist, aber das Behältnis nicht übereinstimmt. Ein Austausch ist nur zwischen identischen Behältnissen möglich – Pen gegen Pen oder Fertigspritze gegen Fertigspritze. Doch auch hier gibt es Unterschiede.
Die einzelnen Devices können unterschiedlich in Handhabung und Aussehen, aber auch in der Füllmenge sein. In der Regel wird der Pen komplett verabreicht, sodass je nach Anbieter auch bei gleicher Dosis unterschiedliche Mengen injiziert werden. Vergleicht man beispielsweise Humira (Amgen) mit Imraldi (Biogen), zeigen sich beim Fertigpen mehrere Unterschiede.
Humira
Der Pen hat eine graue und eine rote Kappe – erst muss die graue, dann die rote abgezogen werden. Dann wird der Fertigpen so gedreht, dass der weiße Pfeil auf dem Fertigpen auf die Körperstelle zeigt, in die das Arzneimittel injiziert werden soll. Dann soll ein Stück der gereinigten Hautfläche mit der freien Hand gegriffen und etwas zusammengedrückt werden. Anschließend wird der Fertigpen mit der weißen Nadelkappe in einem 90-Grad-Winkel auf die Körperstelle aufgesetzt. Dabei ist darauf zu achten, dass der Pen so gehalten wird, dass das Sichtfenster zu sehen ist. Dann den roten Aktivierungsknopf drücken und die Injektion durchführen. Diese startet mit einem Klickgeräusch und ist nach etwa zehn Sekunden beendet, wenn die gelbe Anzeige im Sichtfenster sich nicht mehr bewegt. Wird die Nadel aus der Haut gezogen, schiebt sich die weiße Nadelkappe über die Nadel.
Imraldi
Der Pen hat eine durchsichtige Nadelkappe mit Metall – nachdem diese abgezogen wurde, ist der Pen mit der grünen Basis senkrecht, also in einem Winkel von 90 Grad, auf die gewählte Hautstelle aufzusetzen und der gesamte Pen fest nach unten zu drücken, um die Injektion zu starten. Wird der Pen nach unten gedrückt, beginnt die Injektion. Dabei ist ein erstes Klickgeräusch zu hören. Einen Aktivierungsknopf wie bei Humira gibt es nicht. Der Pen wird so lange gegen die Haut gedrückt, bis der gelbe Indikator das Kontrollfenster ganz ausfüllt und sich nicht mehr bewegt. Erst dann erfolgt ein zweites Klickgeräusch und die Injektion ist beendet.
Compliance beeinflusst
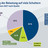
Ergebnisse aus Island, die in der National Library of Medicine veröffentlicht wurden, zeigen, dass die Umstellung von Humira auf Imraldi mit Herausforderungen auf Patientenseite verbunden ist. Dort wurden 2019 Patientinnen und Patienten auf das Biosimilar umgestellt. Knapp die Hälfte (47 Prozent) fand es schwieriger, den Imraldi-Pen zu verwenden als den Humira-Pen, während nur knapp 13 Prozent den Imraldi-Pen leichter in der Anwendung fanden. Hinzukommt, dass die Pens in der Studie ein unterschiedliches Füllvolumen besaßen – 0,4 ml bei Humira und 0,8 ml bei Imraldi. Hierzulande sind die Originalpräparate gleich, es gibt aber Reimporte mit doppeltem Volumen bei gleicher Dosierung.
Unterschiede gibt es also nicht nur in der Anwendung, sondern auch im Gewicht – und bei den sonstigen Bestandteilen: Imraldi enthält Citrat, das zu Beschwerden bei der Injektion führen kann. Bei Humira wird seit 2018 auf Citrat verzichtet.
Apotheken sollen schulen
Apotheken müssen Versicherte zum neuen Device schulen. Die Arzneimittelkommission der Deutschen Apotheker (AMK) weist darauf hin, dass ein wesentliches Risiko durch Anwendungsfehler besteht, die sich beispielsweise aus unterschiedlichen Auslöse- und Sicherheitsmechanismen, variierendem Kraftaufwand bei der Applikation, Entleerungsstörungen oder abweichender Bedienlogik der Applikationssysteme ergeben können. Die Folgen können Fehlanwendungen, unvollständige Applikation oder Unterdosierung sein. Findet in der Apotheke keine entsprechende Beratung statt, kann sich dieses Risiko erhöhen und zudem Verunsicherung bei den Patient:innen entstehen.
„Sofern im Einzelfall eine sichere und sachgerechte Anwendung durch den Patienten nicht gewährleistet erscheint, ist die Prüfung und gegebenenfalls Anwendung pharmazeutischer Bedenken erforderlich“, heißt es von der AMK. Außerdem seien für die Pharmakovigilanz relevante Aspekte zu berücksichtigen: Aufgrund biologischer Variabilitäten könnten Nebenwirkungen chargenspezifisch auftreten. Daher sei bei Spontanberichten eine Chargendokumentation erforderlich.
G-BA sieht kein Problem
Die Verunsicherung der Patient:innen hat der Gemeinsame Bundesausschuss (G-BA) in seinem Beschluss zu § 40c AM-RL berücksichtigt. Können Ärztinnen und Ärzte nicht ausschließen, dass der Austausch mit Risiken verbunden ist, bestehe eine berufsrechtliche Verpflichtung, Gefahren durch Aufklärung oder Ausschluss der Substitution abzuwehren. Die Verpflichtung zur Aufklärung bestehe schon nach § 630c, gegebenenfalls § 630e BGB und der Berufsordnung.
Und auch die Apotheken nimmt der G-BA in die Pflicht: „Soweit eingewendet wird, dass es dadurch bei einem Austausch durch Apotheken zur Verunsicherung der Patientinnen und Patienten kommen könne, ist entgegenzuhalten, dass diese durch adäquate Aufklärung und Beratung vermieden oder gemindert werden kann und nicht dazu führen muss, den Austausch zu unterlassen.“
Die Verpflichtung zur Beratung durch Apotheken bei der Abgabe von Arzneimitteln nach Apothekenbetriebsordnung (ApBetrO) bleibe ebenfalls unberührt. Apotheken müssten ohnehin die Angaben zur Anwendung des Arzneimittels und zu Sicherheitsanforderungen der Fach- und Gebrauchsinformationen grundsätzlich beachten. Die Zusammensetzung hinsichtlich der Hilfsstoffe sei per se kein Kriterium, das zur Bewertung der therapeutischen Vergleichbarkeit herangezogen werden könne. Denn schwere Unverträglichkeiten gegenüber Hilfsstoffen, Patientenpräferenzen und Adhärenzprobleme seien patientenindividuell und könnten bei jeder Arzneimitteltherapie auftreten.
„Die Bedenken hinsichtlich möglicher Anwendungsprobleme der Versicherten bei abweichenden Applikationsmechanismen beziehungsweise Handhabungen unterschiedlicher Devices können zwar für den medizinisch begründeten Einzelfall nachvollzogen werden, werden aber in Bezug auf die grundsätzliche Möglichkeit einer Austauschbarkeit biotechnologisch hergestellter biologischer Fertigarzneimittel nicht geteilt“, heißt es in den tragenden Gründen zum Beschluss. Die Vermeidung von Fehlern bei der Anwendung sei ein wichtiger Teil der ärztlichen Therapie und auch der Beratung in der Apotheke – unabhängig davon, um welches Arzneimittel es sich handele.
Pharmazeutische Bedenken
„Die Möglichkeit der Apotheke, von einer Ersetzung abzusehen, ergibt sich dabei aus § 40c Absatz 5“, so der G-BA. Generell gelte: Ein Ausschluss der Ersetzung von Arzneimitteln aufgrund patientenindividueller und erkrankungsspezifischer Aspekte sei in erster Linie von der verschreibenden Person im Rahmen ihrer Verordnungsentscheidung zu beurteilen.
Allerdings ist aus Sicht des G-BA auch die Apotheke zur Beachtung von Sicherheitsanforderungen aufgrund der Fach- und Gebrauchsinformationen verpflichtet. Dabei könnten sich für die Apotheke patientenindividuelle Aspekte als relevant darstellen, die für die verschreibende Person in Unkenntnis des konkreten, abgegebenen Arzneimittels noch nicht berücksichtigt werden konnten. Dies könnten patientenindividuell relevante Abweichungen hinsichtlich der Injektionsvolumina oder der Handhabung trotz gleicher Behältnisse sein. Diese Aspekte können einer Ersetzung entgegenstehen, wenn die Apotheke durch eine entsprechende Beratung eine Gefährdung des Therapieerfolgs durch Nicht-Adhärenz oder Anwendungsfehler nicht vermeiden kann. Heißt: In diesem Fall kann die Apotheke von einem Austausch des Arzneimittels gemäß § 17 Absatz 5 ApBetrO absehen.
lesen Sie weiter.