BGH soll Lucentis-Streit entscheiden
Den Streit um das Auseinzeln von Lucentis-Fertigspritzen muss der Bundesgerichtshof (BGH) klären: Nachdem das Hanseatische Oberlandesgericht (OLG) im Dezember entschieden hat, dass die Aposan-Tochter Apozyt die Spritzen abfüllen darf, hat Novartis Nichtzulassungsbeschwerde eingelegt. In zwei ähnlichen Verfahren gegen Apotheker Hermann Rohlfs, Inhaber der Privilegierten Rats-Apotheke in Uslar, sollte heute eigentlich eine Entscheidung verkündet werden – doch nun könnte das Verfahren ausgesetzt werden.
In den Prozessen geht es um die grundsätzliche Frage, ob beim Abfüllen eines Fertigarzneimittels ein neues Medikament entsteht – und der Abfüller daher eine eigene Zulassung braucht. Zwei EU-Vorgaben stehen nebeneinander: Die EU-Verordnung 726/2004 schreibt vor, dass bestimmte Arzneimittel nur dann in den Verkehr gebracht werden dürfen, wenn dafür eine Genehmigung erteilt wurde. Demgegenüber stehen die EU-Richtlinie zu Humanarzneimitteln 2001/83/EG und das deutsche Apothekengesetz, die Ausnahmen für Rezepturen vorsehen.
Zunächst hatte es für Apozyt gut ausgesehen: Der eingeschaltete Europäische Gerichtshof (EuGH) hatte im April 2013 klargestellt, dass eine Zulassung nicht erforderlich ist, wenn die Umfüllung nicht zu einer Veränderung des Arzneimittels führt und nur auf der Grundlage individueller Verordnungen vorgenommen wird. Die Bewertung des konkreten Falls überließen die Richter in Luxemburg aber den Kollegen in Hamburg.
Das Landgericht (LG) legte den Begriff „Veränderung“ sehr weit aus: Er umfasse neben Änderungen der Substanz oder des Wirkstoffes auch Änderungen bei Dosierung, Darreichungsform, Anwendung und Haltbarkeit, hieß es in der Urteilsbegründung. Messen lassen muss sich die Rezepturherstellung demnach an den Vorgaben, die für den Originalhersteller gelten würden.
Genauso bewerteten die Richter in der mündlichen Verhandlung auch die Auseinzelung durch die Privilegierte Rats-Apotheke. Rohlfs musste sich gegen Novartis und Bayer verteidigen, weil er nicht nur Lucentis (Ranibizumab), sondern auch Eylea (Aflibercept) ausgeeinzelt hatte. Er hatte sich darauf bezogen, dass für Rezepturen aus Apotheken keine Zulassung benötigt werde.
In der Verhandlung machten die Richter deutlich, dass die EU-Verordnung aus ihrer Sicht keine Ausnahme für Rezepturen vorsieht. Und da das Ausgangsprodukt verändert werde, brauche Rohlfs eine Zulassung. Der Apotheker wandte ein, dass ein Verbot von Zubereitungen aus biotechnologisch hergestellten Fertigarzneimitteln dramatische Folgen hätte, etwa für die Restmengenverwertung im Bereich der Zytostatika.
Die Urteilsverkündung war wiederholt verschoben worden – und zwischenzeitlich hatte im Apozyt-Verfahren bereits die zweite Instanz entschieden. Die Richter am OLG bewerteten den Fall anders als ihre Kollegen: Aus ihrer Sicht ist das EuGH-Urteil so zu verstehen, dass sich die Zusammensetzung eines Arzneimittels nicht verändern darf. Dass Änderungen bei der Haltbarkeit oder der Darreichungsform gemeint gewesen seien, konnten die Richter der Entscheidung nicht entnehmen.
Das Urteil ist noch nicht rechtskräftig, denn Novartis hat einem Gerichtssprecher zufolge Nichtzulassungsbeschwerde eingelegt. Nun muss sich der BGH mit dem Fall befassen. Zunächst muss er entscheiden, ob die Beschwerde zulässig ist.
Das hat auch für das Verfahren gegen Rohlfs Folgen: Eigentlich wollte das LG heute sein Urteil verkünden. Dazu kam es aber nicht. Stattdessen soll die Sache einem Gerichtssprecher zufolge noch einmal erörtert werden. Es könnte sein, dass das Verfahren bis zu einem letztinstanzlichen Urteil ausgesetzt wird.
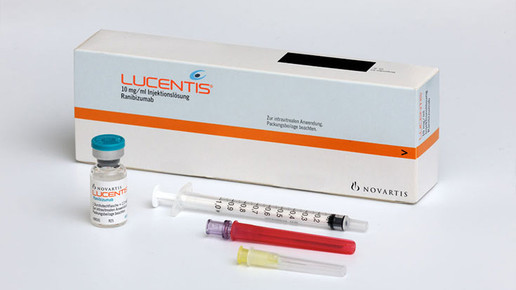
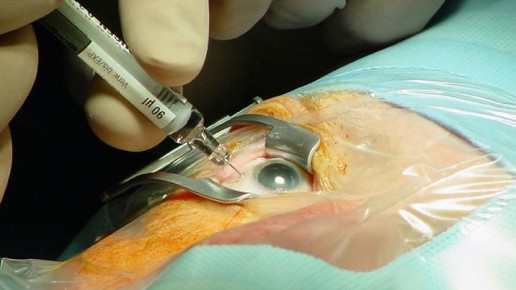
Lucentis wurde von Novartis lange nur in Durchstechflaschen mit 0,23 Millilitern Inhalt vertrieben. Für die Behandlung verwenden Ärzte aber lediglich 0,05 Milliliter – der Rest wird verworfen. Apozyt hatte unter sterilen Bedingungen die für eine Injektion nötige Menge abgefüllt. Auf diese Weise konnten die Therapiekosten deutlich reduziert werden. Novartis vertrat die Ansicht, für die Herstellung von Fertigspritzen benötige Apozyt eine Zulassung, und klagte.
Zwischenzeitlich hatten sich Apozyt und Novartis darauf verständigt, bis zum Abschluss des Berufungsverfahrens keine Spritzen mehr auszueinzeln, sondern stattdessen die neuen Fertigspritzen des Originalherstellers mit 0,165 ml Inhalt zu vertreiben. Seit der Entscheidung des OLG im Dezember werden in Köln aber bereits wieder Originalspritzen ausgeeinzelt.





































APOTHEKE ADHOC Debatte