Das Ende vom Anfang? Wenn Ärzte ihre Patienten wegen der Rückrufwelle umstellen, könnte das das Aus für Valsartan bedeuten.
Foto: APOTHEKE ADHOC
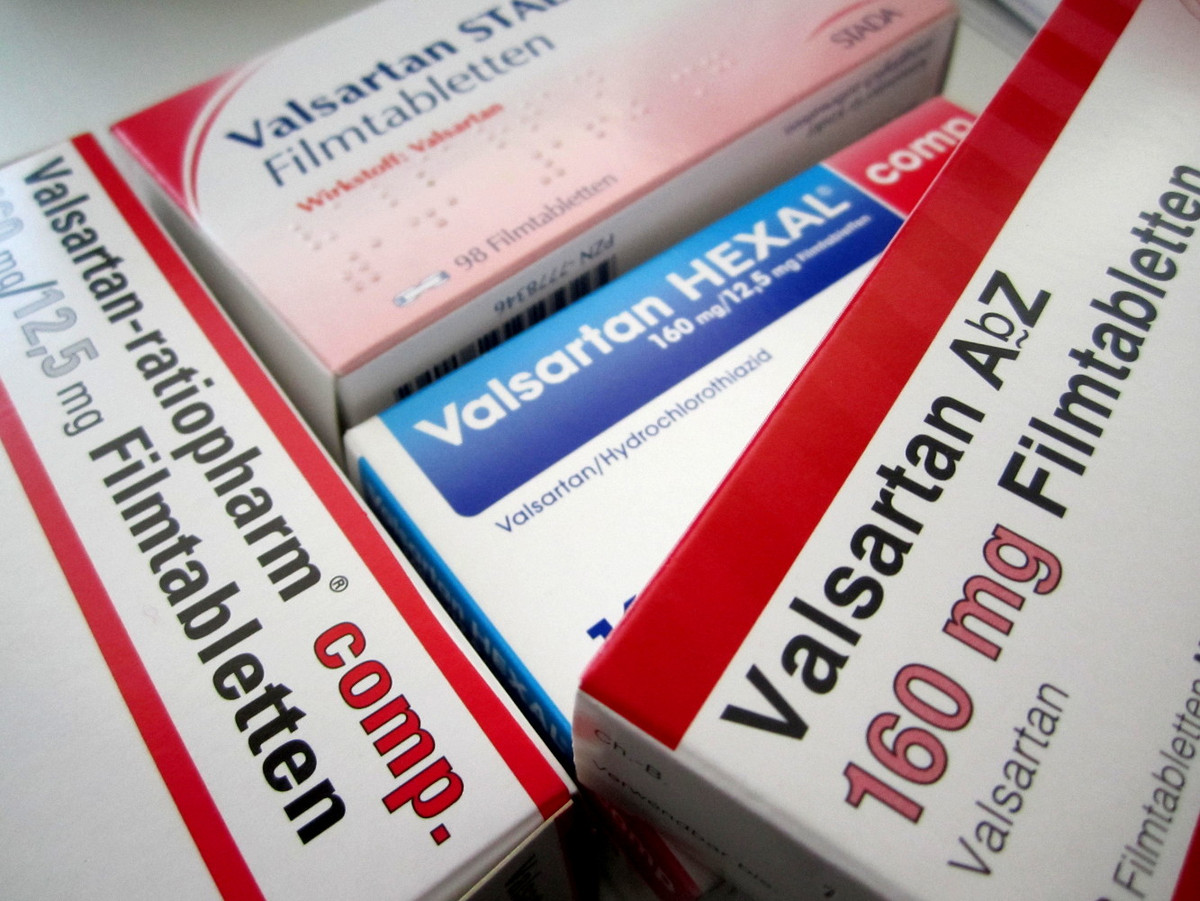
Seit Jahren verunreinigt? Hinter den Problemen bei Valsartan könnte sich ein Arzneimittelskandal verbergen.
Foto: APOTHEKE ADHOC

Die Welle rollt: Mehrere Hersteller riefen Valsartan zurück, darunter Stada/Aliud, ...
Foto: APOTHEKE ADHOC
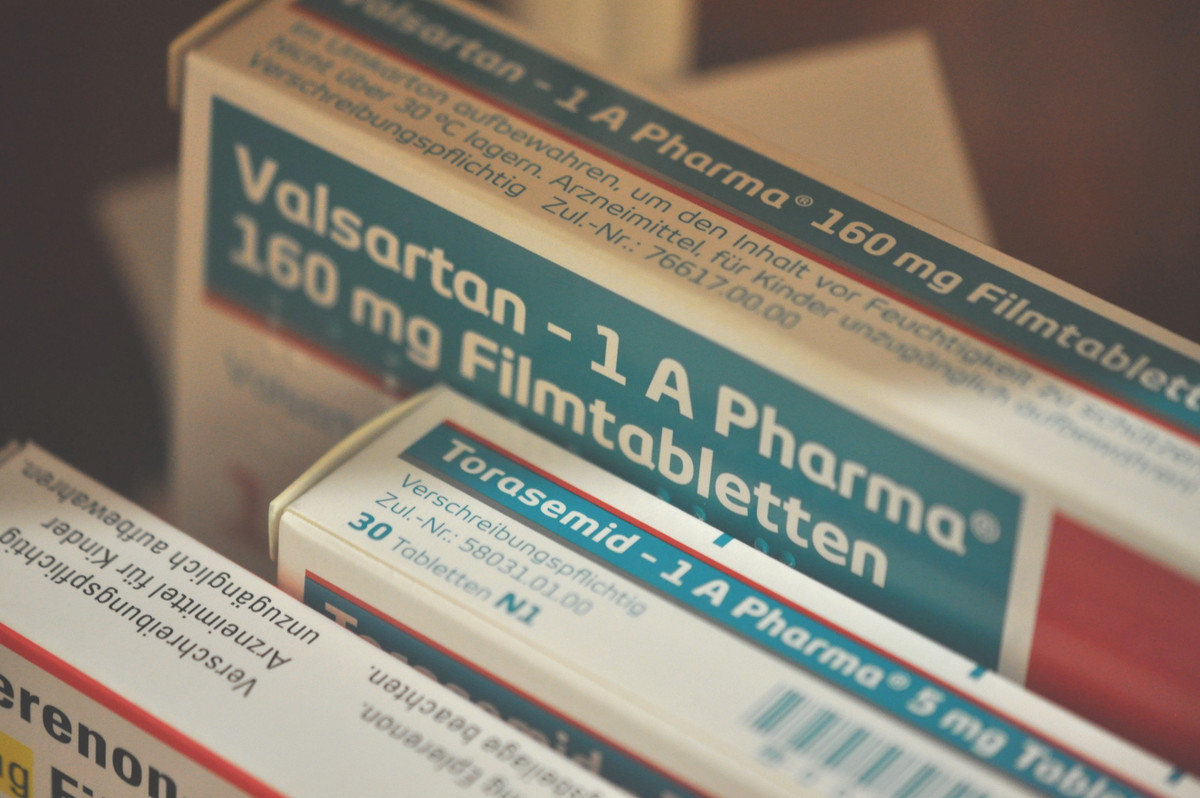
... Hexal/1A und ...
Foto: APOTHEKE ADHOC
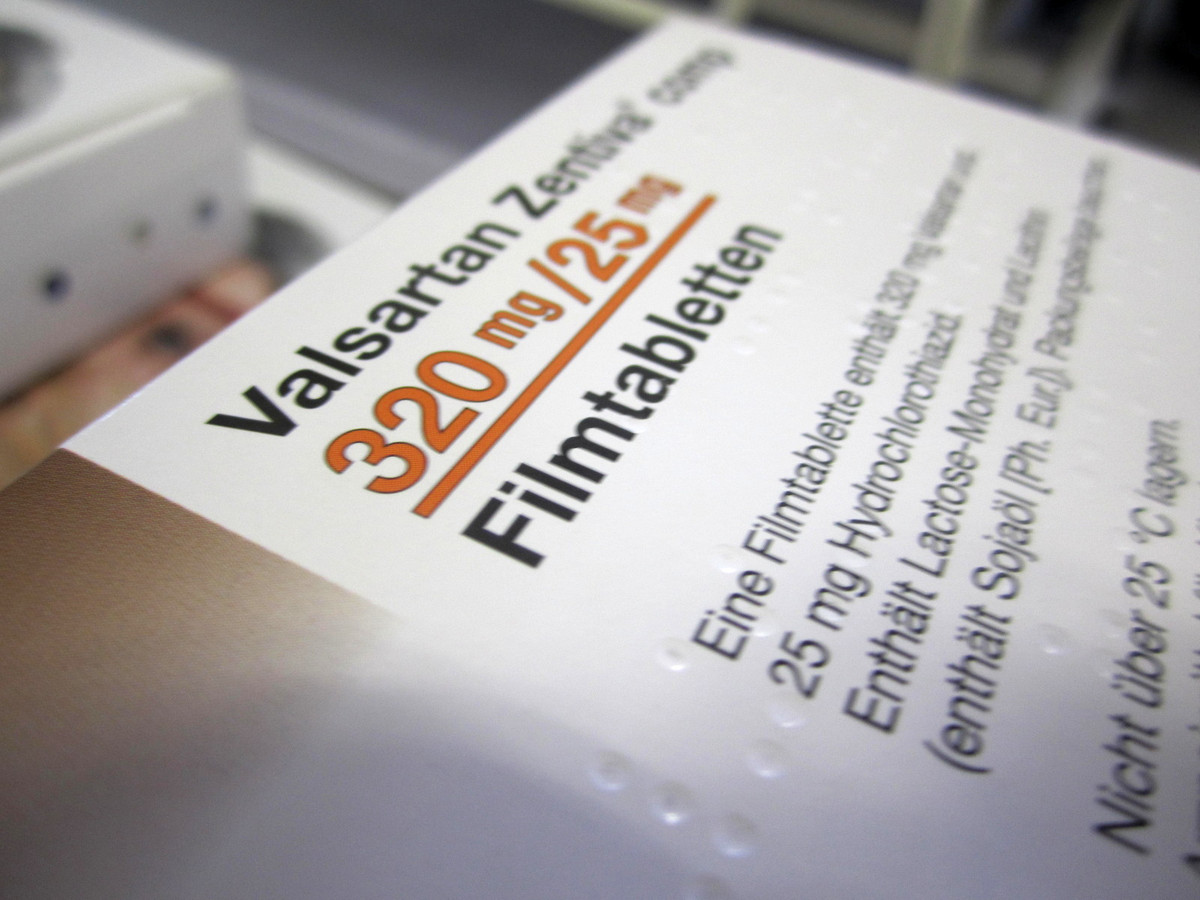
... Zentiva.
Foto: APOTHEKE ADHOC

Einen Rückruf gab es auch von Ratiopharm/AbZ.
Foto: APOTHEKE ADHOC

Weitere Anweisungen der AMK sollen folgen.
Foto: APOTHEKE ADHOC

Nicht betroffen: TAD ist mit Valsacor Rabattpartner vieler Kassen – und von der Verunreinigung nicht betroffen.
Foto: APOTHEKE ADHOC

Auch Mylan ist nicht betroffen, da der Wirkstoff hier aus Indien kommt.
Foto: APOTHEKE ADHOC

Novartis produziert Diovan & Co. selbst in Irland und in der Schweiz und muss daher ebenfalls nichts zurückrufen.
Foto: APOTHEKE ADHOC

In den Apotheken warten die Packungen jetzt darauf, zurückgeschickt zu werden.
Foto: APOTHEKE ADHOC

Damit droht den Apotheken erneut eine Rückrufliste wie auch schon 2016.
Foto: Andreas Domma

Apotheken bekommen es schon jetzt mit verunsicherten Kunden zu tun.
Foto: Elke Hinkelbein

Gefälschte Studien: Die EMA hatte zuletzt 370 Zulassungen geprüft, die auf Daten von Micro Therapeutic Research beruhten.
Foto: Micro Therapeutic Research

Es war bereits das fünfte Mal, dass ein indischer Studiendienstleister in die Kritik gerät.
Foto: Amar Archtitecture

In der Kritik stand zuvor Semler Research. Das Unternehmen musste sich gegenüber EMA, FDA und WHO verteidigen.
Foto: Elke Hinkelbein

Das BfArM hatte im Sommer 2016 elf Generika aus dem Verkehr gezogen, deren Zulassung auf Daten von Semler beruhten.
Foto: APOTHEKE ADHOC

Der Stopp galt zunächst für ein Jahr. Hexal und die Konzerntochter 1A Pharma waren zahlenmäßig am stärksten vertreten.
Foto: APOTHEKE ADHOC

Auch zwei Generika von Ratiopharm – Atovaquon/Proguanilhydrochlorid in den Stärken 62,5 mg/25 mg und 250 mg/100 mg (Filmtabletten) – mussten vom Markt.
Foto: Glenmark

Ferner vom Ruhen der Zulassung betroffen war Celecoxib von Glenmark (Hartkapseln mit 100 und 200 mg).
Foto: APOTHEKE ADHOC

Insgesamt wurde 2015 für rund 700 Zulassungen das Ruhen der Zulassung empfohlen.
Foto: EMA

Auch der indische Dienstleister Alkem stand schon unter Verdacht. Er soll Elektrokardiogramme für Bioäquivalenzstudien manipuliert haben.
Foto: Alkem

Allerdings waren keine Produkte in Deutschland betroffen.
Foto: Alkem

1973 gegründet, hat sich Alkem mit Hauptsitz in Mumbai auf Generika spezialisiert.
Foto: Alkem

Zum Portfolio gehören unter anderem Antiinfektiva, Präparate für die Schmerztherapie, Nahrungsergänzungsmittel und auch Immunsuppressiva.
Foto: Alkem

Insgesamt werden 705 Produkte im Porfolio geführt.
Foto: Alkem

Alkem gehört damit in Indien zu den Top-10-Pharmaunternehmen.
Foto: Alkem

Das Unternehmen hat 16 Produktionsstätten, 14 in Indien und zwei in den USA.
Foto: Alkem

Die bei Alkem produzierten Generika werden in Indien und 55 weiteren Ländern vermarktet.
Foto: Alkem

Im Sommer 2015 hatte die WHO eine Verwarnung an das indische Unternehmen Quest Life Sciences ausgesprochen.
Foto: WHO

Den größten Skandal gab es 2014 kurz vor Weihnachten: Die französische Arzneimittelbehörde ANSM erhob Vorwürfe gegenüber dem Dienstleister GVK Biosciences.
Foto: GVK Biosciences

Die Ernsthaftigkeit der Mängel und das Fehlen von GCP-Compliance hätten Zweifel an der Glaubwürdigkeit aller Studien des Dienstleisters aufgeworfen.
Foto: GVK Biosciences

Die Behörde hatte daher entschieden, dass die Studien nicht der Guten klinischen Praxis (GCP) entsprechen und nicht Grundlage für Marktzulassungen sein können.
Foto: GVK Biosciences

GVK Biosciences ist nach eigenen Angaben einer der größten Anbieter für Auftragsforschung in Asien.
Foto: GVK Biosciences

Der Dienstleister beschäftigt demnach 2400 Mitarbeiter und hat mehr als 300 Kunden, darunter auch Konzerne, die unter den Top 10 der Branche sind.
Foto: GVK Biosciences

Im April 2015 hatte Neu-Delhi mit rechtlichen Schritten gegen die EU gedroht. Laut indischer Regierung hatte GVK Biosciences die Bioäquivalenzstudien nicht gefälscht.
Foto: GVK Biosciences

Eine von der indischen Regierung eingesetzte unabhängige Expertengruppe habe bewiesen, dass die Studien nicht manipuliert wurden.
Foto: GVK Biosciences

Indien forderte von der EMA, die Aufhebung zu überdenken.
Foto: APOTHEKE ADHOC

Diese hatte GVK vorgeworfen, systematisch vorzugehen.
Foto: GVK Biosciences

Die EMA hatte die Hersteller aufgefordert, anzugeben, ob und bei welchen Arzneimitteln GVK beauftragt wurde.
Foto: GVK Biosciences

Das BfArM hatte Anfang Dezember 2014 eine Liste mit 80 Zulassungen veröffentlicht, für die das Ruhen der Zulassung angeordnet worden war – darunter auch Tacpan. Der Hersteller legte Widerspruch ein.
Foto: APOTHEKE ADHOC

Mit der kombinierten EMA/BfArM-Liste vom 21. August 2015 ruhten insgesamt 54 Zulassungen.
Foto: APOTHEKE ADHOC

Candesartan von Mylan dura stand zwar weder auf der BfArM- noch auf der EMA-Liste; der Hersteller veranlasste aber selbst einen Rückruf.
Foto: APOTHEKE ADHOC

Zurückgerufen wurde auch Esomeprazol dura.
Foto: APOTHEKE ADHOC

Ursprünglich standen Candesartan/HCT, Irbesartan/HCT und Venlafaxin von Heumann auf der Liste. Für diese Wirkstoffe konnte der Hersteller die Zweifel aber aus der Welt schaffen.
Foto: APOTHEKE ADHOC

Auch Mylan und Fair-Med hatten den BfArM-Bescheiden widersprochen.
Foto: APOTHEKE ADHOC

Auf der BfArM-Liste standen auch Arzneimittel, die zwar zugelassen wurden, aber niemals in den Handel gelangt sind – beispielsweise Entacapon von Stada.
Foto: Elke Hinkelbein

Von der Sperre des BfArM waren nicht alle genannten Arzneimittel betroffen, sondern jeweils nur eine Zulassung.
Foto: APOTHEKE ADHOC

Ob ein Arzneimittel abgegeben werden durfte oder nicht, hing von der jeweils aktuellen Liste ab.
Foto: APOTHEKE ADHOC

„Unterschiedliche Fristen und Verfahren werden dazu führen, dass das Ruhen der Zulassung bestimmter Produkte jederzeit und in unregelmäßigen Abständen vom BfArM aufgehoben werden kann“, teilte die Behörde mit.
Foto: Elke Hinkelbein

Levetiracetam von Betapharm wurde erst im Januar 2016 von der BfArM-Liste gestrichen.
Foto: APOTHEKE ADHOC

Im Dezember 2014 wurde die erste BfArM-Liste veröffentlicht, am Ende standen noch 46 Präparate darauf.
Foto: Elke Hinkelbein

Für Tacrolimus hatte das BfArM eine Ausnahme gemacht.
Foto: Elke Hinkelbein

Tacpan durfte weiter abgegeben werden, obwohl das Präparat auf der BfArM- und der EMA-Liste stand.
Foto: APOTHEKE ADHOC

Allerdings wurde Tacpan vom BfArM als Arzneimittel bewertet, dass für Patienten „eine entscheidende Bedeutung“ hat.
Foto: Elke Hinkelbein

Auch der Gesundheitsausschuss des Bundestags hatte sich mit den Maßnahmen des BfArM beschäftigt.
Foto: Elke Hinkelbein

Kathrin Vogler (Linke) kritisierte Arzneimittelstudien in Indien als „Medikamenten-Imperialismus“.
Foto: Christof Stache

ABDA-Präsident Friedemann Schmidt sah die Ursache des Problem in der Globalisierung.
Foto: Elke Hinkelbein

DAV-Chef Fritz Becker kündigte an, sich mit den Kassen wenigstens in Sachen möglicher Retaxationen geeinigt zu haben.
Foto: Elke Hinkelbein

Magdalene Linz, Präsidentin der niedersächsischen Apothekerkammer, forderte, die Herstellung wieder vermehrt nach Europa zu verlagern.
Foto: Elke Hinkelbein