Von Andexanet bis Vortigen
Das waren die Arzneimittel-Innovationen 2019
Berlin -
2019 wurden 25 Medikamente mit neuem Wirkstoff zugelassen – 11 weniger als im vergangenen Jahr. Zehn Arzneistoffe wurden im Indikationsbereich Onkologie eingeführt. Das waren die Innovationen 2019.
Andexanet alfa – Ondexxya (Portola Phamraceuticals)
- Zulassung im September
- Indikation: Antidot zu Faktor Xa-Hemmern
- Zur Behandlung akuter Blutungen bei Patienten, die mit den Faktor-Xa-Hemmern Rivaroxaban oder Apixaban oder mit niedermolekularem Heparin behandelt werden.
Anthrax-Impfstoff adsorbiert – BioThrax (Emergent BioSolutions)
- Zulassung im Mai
- Indikation: Vorbeugung von Milzbrand
- Zur Aktivierung des Immunsystems bei Patienten die einem potentiellem Risiko einer Ansteckung mit Anthrax (Milzbrand) ausgesetzt sind. Zur vollen Immunisierung werden drei Dosen benötigt.
Apalutamid – Erleada (Janssen-Cilag)
- Zulassung im Februar
- Indikation: Prostata-Karzinom, nicht metastasiert
- Bei dem Wirkstoff handelt es sich um einen Androgenrezeptor- und Östrogenrezeptor-Antagonisten.
Brigatinib – Alunbrig (Takeda)
- Zulassung im Januar
- Indikation: Lungenkrebs, nicht-kleinzelliger
- Der Wirkstoff hemmt die Phosphorylierung von Signalproteinen und damit die Vermehrung der Krebszellen
- Einsatz nur bei ALK-positivem Tumor (ALK = anaplastische Lymphomkinase)
Cemiplimab – Libtayo (Sanofi Genzyme und Regeneron)
- Zulassung im August
- Indikation: Plattenepithelkarzinom der Haut
- Der monoklonale Antikörper richtet sich gegen PD-1 – es handelt sich um einen Immuncheckpoint-Inhibitor.
- Anwendung bei metastasiertem und lokal fortgeschrittenem Hautkrebs
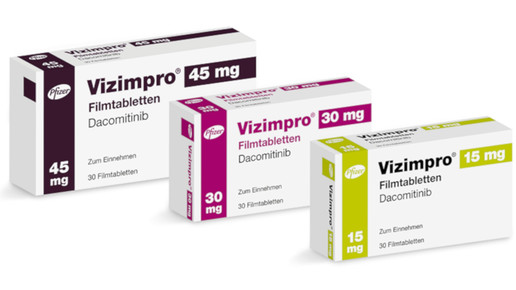
Dacomitinib – Vizimpro (Pfizer)
- Zulassung im Mai
- Indikation: Lungenkrebs, nicht-kleinzelliger (NSCLC)
- Der Wirkstoff hemmt irreversibel die EGFR-Tyrokinase – Hemmung der HER1, HER2 und HER4-Rezeptoren.
Damoctocog alfa pegol Jivi (Bayer)
- Zulassung im Januar
- Indikation: Behandlung und Prophylaxe bei Hämophilie A
- Es handelt sich um einen langwirksamen pegylierten rekombinanten Faktor VIII ohne B-Domäne.
Doravirin – Pifeltro (MSD)
- Zulassung im Januar
- Indikation: HIV 1-Infektion
- Es handelt sich um einen nicht-nukleosidischen reversen Transkriptasehemmer.
- Die Anwendung erfolgt in Kombination mit weiteren antiretroviralen Arzneimitteln.
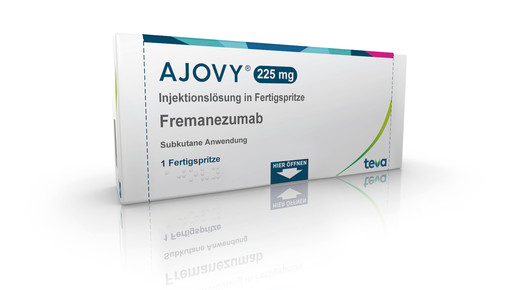
Fremanezumab – Ajovy (Teva und Pfizer)
- Zulassung im Mai
- Indikation: Migräneprophylaxe
- Der monoklonale Antikörper richtet sich gegen das Calcitonin Gen-bezogene Peptid (CGRP).
- Die Anwendung erfolgt subkutan als Injektion alle drei Monate.
Galcanezumab – Emgality (Lilly)
- Zulassung im April
- Indikation: Migräneprophylaxe
- Der Wirkstoff richtet sich gegen das Calcitonin Gen-bezogene Peptid (CGRP).
- Die Anwendung erfolgt subkutan als Injektion einmal im Monat.
Giltertinib – Xospata (Astellas)
- Zulassung im Dezember
- Indikation: Leukämie, akute myeloische
- Der FLT3-Antagonist ist gleichzeitig ein Axl-Rezeptor-Kinase-Hemmer, der sich gegen FLT3mut+ richtet.
- Zulassung als Orphan Drug
Lanadelumab – Takhzyro (Shire)
- Zulassung im Februar
- Indikation: Anioödem, hereditäres
- Der monoklonale Antikörper hemmt das Enzym Plasma-Kallikrein und dient der Vorbeugung wiederkehrender Anfälle.
- Die Anwendung erfolgt subkutan als Injektion alle zwei Wochen.
- Zulassung als Orphan Drug
Larotrectinib – Vitrakvi (Bayer)
- Zulassung im Oktober
- Indikation: solide Tumor emit NTRK-Genfusion
- Der Wirkstoff hemmt die neurotrophe TR-Kinase
- Besonerheit: Erstes Arzneimittel, welches tumorunabhängig zugelassen wurde – jeder Tumor, der mit einer bestimmten Genmutation in Verbindung steht, kann mit Vitrakvi behandelt werden.
Lorlatinib – Lorviqua (Pfizer)
- Zulassung im Juni
- Indikation: Lungenkrebs, nicht-kleinzelliger (NSCLC)
- Der ALK/ROS1-Hemmer kann nur bei ALK-positiven Tumoren eingesetzt werden.
- Zulassung über Härtefallantrag
Nerapatinib – Nerlynx (Puma Biotech)
- Zulassung im Dezember
- Indikation: Brustkrebs
- Der Wirkstoff hemmt mehrere Kinasen in den Tumorzellen.
- Der Arzneistoff kann bei adjuvanten, vorbehandelten Patientinnen eingesetzt werden – ein Vortest auf HER2-Status ist erforderlich.
Pegvaliase – Palynziq (BioMarin)
- Zulassung im Juli
- Indikation: Phenylketonurie
- Die pegylierte Version des Enzyms Phenylalanin-Ammoniumlyase baut Phenylalanin ab.
- Zulassung als Orphan Drug
Ravlizumab – Ultomiris (Alexion)
- Zugelassen im August
- Indikation: Paroxysmale nächtliche Hämoglobinurie
- Der monoklonale Antikörper richtet sich gegen den Komplementfaktor C5.
- Die Verabreichung erfolgt alle acht Wochen – der Arzneistoff ist länger wirksam als vergleichbare Therapien.
Risankizumab – Skyrizi (AbbVie)
- Zugelassen im Juni
- Indikation: Psoriasis
- Der IL23-Hemmer bindet an die p19-Untereinheit des Interleukins, dadurch erfolgt eine Neutralisierung.
- Eine Injektion erfolgt einmal pro Quartal.
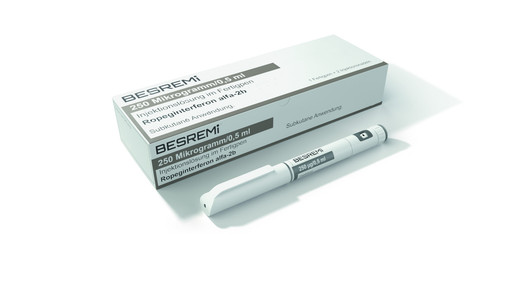
Robeginterferon alfa-2b – Besremi (AOP Orphan)
- Zugelassen im September
- Indikation: Polycythaemia vera
- Der Wirkstoff hebt die Wirkung von Zytokinen auf Wachstumsfaktoren auf (Myelofibrosen assoziiert) und hemmt die Proliferation von Vorläuferzellen im Knochenmark.
Rucaparib – Rubraca (Clovis)
- Zugelassen im März
- Indikation: Eierstock-Krebs, Eileiter-Krebs, Peritoneal-Krebs
- Der Wirkstoff hemmt die Enzyme der Poly(ADP-Ribose)-Polymerase.
- Es handelt sich um einen personalisierten Ansatz: Vortest auf BRCA-Mutation im Tumorgewebe nötig.
Temocillin – Temopen (Eumedica)
- Zugelassen im Oktober
- Indikation: Infektionen mit gramnegativen Bakterien
- Das Penicillin-Antibiotikum wird insbesondere bei Infektionen der Harnwege, der unteren Atemwege und bei infizierten Wunden eingesetzt.
- Das Arzneimittel besitzt eine Resistenz gegen Betalactamasen der Klassen A und C.
- In der EU in vielen Ländern seit längerer Zeit zugelassen – in Deutschland erfolgte die Markteinführung aufgrund der Anerkennung der belgischen Zulassung.
Turoctocoq alfa pegol – Esperoct (Novo Nordisk)
- Zugelassen im August
- Indikation: Hämophilie A
- Es handelt sich um eine Weiterentwicklung des Wirkstoffes Turoctocoq alfa.
- Der Faktor XIII wird zur Prophylaxe angewendet – durch die Glykan-Pegylierung ist eine Verabreichung jeden vierten Tag ausreichend.
Volanesorsen – Waylivra (Akcea)
- Zugelassen im August
- Indikation: Familiäres Chylomikronämie-Syndrom
- Der Arzneistoff ist ein Antisense-Oligonukleotid, welches das Apolipoprotein C3-hemmt.
Vonicoq alfa – Veyvondi (Shire)
- Zugelassen im Januar
- Indikation: von-Willebrand-Syndrom
- Es handelt sich um einen gereinigten, rekombinanten, humanen von-Willebrand-Faktor (rVWF).
Vortigen neparvovec – Luxturna (Spark / Novartis)
- Zugelassen im April
- Indikation: Erblindung durch Lebersche kongenitale Amaurose oder Retinis pigmentosa
- Der Wirkstoff ist ein Adeno-assoziierter Virus-Vektor mit dem korrekten RPE65-Gen – die Adenoviren infizieren die Zellen und bringen so die Kopie des Gens ein, als Folge können Enzyme wieder korrekt gebildet werden.
- Es handelt sich um eine personalisierte Anwendung, eine biallische Mutation im RPE65-Gen muss vorliegen.
- Zulassung als Orphan Drug
Newsletter
Das Wichtigste des Tages direkt in Ihr Postfach. Kostenlos!
Lesen Sie auch
Neuere Artikel zum Thema
Mehr zum Thema
Neue Therapieoption
Netilmicin gegen bakterielle Augeninfektion
Prostatakrebs
Pluvicto: Novartis plant Zulassungserweiterung
Hoffnung für Millionen Menschen
Kaliumkanalblocker: Nasenspray gegen Schlafapnoe
Mehr aus Ressort
Dosierung beachten
Gegen Versorgungsmangel: Irenat aus Österreich
Defekteliste des BfArM
Isoket Sublingual: Engpass bis zum Jahr 3000?
Krebsmittel
Roche erhält für Alecensa US-Zulassung
































APOTHEKE ADHOC Debatte