Covid-19: Neue Remdesivir-Daten liegen vor
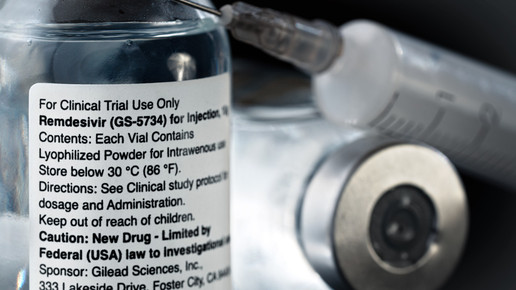
Gilead hat heute zusätzliche Daten zu Remdesivir bekannt gegeben. Bisher ist das Präparat das einzige in der EU-zugelassene Medikament zur Behandlung von Covid-19. Die Daten umfassen eine vergleichende Analyse der Phase-III-Simple-Severe-Studie und eine reale retrospektive Kohorte von Patienten mit schweren Covid-Verläufen.
Remdesivir wurde in der vergangenen Woche in Europa zur Behandlung von Covid-19 zugelassen. Die EU-Kommission hat der bedingten Zulassung von Remdesivir zugestimmt. Das antivirale Mittel ist in den USA und in Japan bereits auf dem Markt. Die Gabe von Remdesivir soll eine Hospitalisierung im Schnitt um vier Tage verkürzen. Die aktuell zusätzlich präsentierten Daten zeigen, dass eine Behandlung mit dem antiviralen Mittel die klinische Genesung auch in der Praxis verbessert.
Kinder und Schwangere
Aus Analysen des Compassionate-Use-Programms konnte gezeigt werden, dass 83 Prozent der pädiatrischen Patienten (n = 77) und 92 Prozent der schwangeren Frauen (n = 86) bis zum 28. Tag wieder gesund wurden. In diesen Populationen wurden keine neuen Nebenwirkungen mit Remdesivir identifiziert. Gilead kündigte kürzlich die Einleitung einer globalen, offenen Phase-II/III-Studie an, um die Sicherheit, Verträglichkeit und Pharmakokinetik von Remdesivir bei pädiatrischen Patienten von der Geburt bis zu einem Alter von unter 18 Jahren zu bewerten. Gilead arbeitet auch an einer Studie für schwangere Frauen.
„Wir arbeiten daran, unser Verständnis für den vollen Nutzen von Remdesivir zu erweitern. Um der Dringlichkeit der anhaltenden Pandemie zu begegnen, teilen wir so schnell wie möglich Daten mit der Forschungsgemeinschaft, um transparente und zeitnahe Aktualisierungen neuer Entwicklungen mit Remdesivir bereitzustellen“, sagte Dr. Merdad Parsey, Chief Medical Officer bei Gilead. „Diese auf der virtuellen Covid-19-Konferenz vorgestellten Daten werfen ein zusätzliches Licht auf die Verwendung von Remdesivir bei bestimmten Patientenpopulationen, einschließlich solcher, die möglicherweise für höhere Covid-19-Infektionsraten anfällig sind, sowie anderer besonders gefährdeter Patienten, einschließlich Kinder und Schwangere und stillende Frauen. “
Vergleich mit retrospektiver Kohorte
Bei der vergleichenden Analyse der Phase-III-Simple-Severe-Studie und der realen retrospektiven Kohorte von Patienten, bei denen ein schwerer Covid-19-Standard diagnostiziert wurde, konnte zusammenfassend vor allem gezeigt werden, dass die Behandlung mit Remdesivir mit einer signifikant verbesserten klinischen Erholung und einer Verringerung des Mortalitätsrisikos um 62 Prozent im Vergleich zum Standard der Behandlung verbunden war.
Die meisten Probanden stammen aus Nordamerika
Die vergleichende Analyse umfasste 312 Patienten, die in der Simple-Severe-Studie der Phase III behandelt wurden, und eine separate retrospektive Kohorte von 818 Patienten mit ähnlichen Ausgangsmerkmalen und Schweregraden der Erkrankung. Örtlich befanden sich die Patienten befanden hauptsächlich in Nordamerika (92 Prozent Remdesivir-Kohorte gegenüber 91 Prozent Standard-of-Care-Kohorte), Europa (5 gegenüber 7 Prozent) und Asien (3 vs. 2 Prozent).
Die Analyse zeigte, dass die Behandlung mit Remdesivir mit einer signifikant verbesserten klinischen Erholung und einer Verringerung des Mortalitätsrisikos um 62 Prozent im Vergleich zum Standard der Behandlung verbunden war. Die Ergebnisse der vergleichenden Analyse zeigten, dass sich 74,4 Prozent der mit Remdesivir behandelten Patienten bis zum 14. Tag erholten, während 59 Prozent der Patienten mit einer Standardbehandlung diesen Endpunkt erreichten. Die Genesung wurde als Verbesserung des klinischen Status auf der Grundlage einer 7-Punkte-Ordnungsskala definiert. Die Mortalitätsrate für Patienten, die in der Analyse mit Remdesivir behandelt wurden, betrug 7,6 Prozent an Tag 14, verglichen mit 12,5 Prozent bei Patienten, die kein Remdesivir einnahmen. „Diese vergleichende Analyse liefert wertvolle zusätzliche Informationen zum Nutzen von Remdesivir im Vergleich zum alleinigen Pflegestandard“, sagte Dr. Susan Olender vom Irving Medical Center der Columbia University. „Diese Analyse ist zwar nicht so aussagekräftig wie eine randomisierte kontrollierte Studie, basiert jedoch auf einer realen Umgebung und dient als wichtige Ergänzung zu Daten klinischer Studien. Sie trägt zu unserem kollektiven Verständnis dieses Virus bei und spiegelt das außergewöhnliche Tempo der anhaltenden Pandemie wider.”
Phase-III-Simple-Severe-Studie
In der Phase-III-Simple-Severe-Studie wurde die Sicherheit und Wirksamkeit der intravenösen Verabreichung von Remdesivir über fünf und zehn Tage bei Krankenhauspatienten mit schweren Manifestationen von Covid-19 bewertet. In der Anfangsphase der Studie wurden 397 Patienten im Verhältnis 1:1 randomisiert, um zusätzlich zum Standard der Behandlung eine Behandlung mit Remdesivir zu erhalten. Die Ergebnisse wurden im Mai im „New England Journal of Medicine“ (NEJM) veröffentlicht. Eine Expansionsphase der Studie wurde hinzugefügt, um bis zu 5600 zusätzliche Patienten aufzunehmen, einschließlich Patienten mit mechanischer Beatmung. Ergebnisse aus der Expansionsphase stehen noch aus.
Remdesivir plus Hydroxychloroquin
Nachdem In-vitro-Daten verfügbar waren, die belegen, dass Hydroxychloroquin die antivirale Aktivität von Remdesivir dosisabhängig hemmt, führte Gilead eine Analyse der klinischen Ergebnisse bei Patienten durch, die gleichzeitig mit Remdesivir und Hydroxychloroquin behandelt wurden. Verglichen wurden die Ergebnisse mit denen von Patienten, die ausschließlich mit Remdesivir behandelt wurden. Bei einer medianen Nachbeobachtungszeit von 14 Tagen waren die Rate und die Wahrscheinlichkeit einer Genesung bei Patienten, die gleichzeitig Hydroxychloroquin erhielten, niedriger als bei Patienten, die nur mit Remdesivir behandelt wurden.
Auswirkungen der ethnischen Herkunft
Weitere neue Daten zur Sicherheit und Wirksamkeit von Remdesivir, die vorgestellt wurden, umfassen Untergruppenanalysen, einschließlich der ethnischen Zugehörigkeit von in den USA behandelten Patienten sowie globale Basismerkmale im Zusammenhang mit einem verbesserten klinischen Status und der gleichzeitigen Anwendung von Hydroxychloroquin. In dieser Studie wurden 229 Patienten an Versuchsstandorten in den USA eingeschlossen. Die klinische Verbesserung wurde als ≥ 2-Punkt-Verbesserung auf einer 7-Punkt-Ordnungsskala definiert. Unter diesen Patienten betrug die klinische Verbesserungsrate am 14. Tag 84 Prozent bei afroamerikanischen Patienten (n = 43), 76 Prozent bei hispanisch weißen Patienten (n = 17), 67 Prozent bei asiatischen Patienten (n = 18). 67 Prozent bei nicht-hispanischen weißen Patienten (n = 119) und 63 Prozent bei Patienten, die sich mit keiner dieser Gruppen identifizierten (n = 32).




















APOTHEKE ADHOC Debatte