Chaos in der Sichtwahl
Warnhinweise auf Analgetika sollen die Patientensicherheit erhöhen, doch stattdessen gibt es Verwirrung und Chaos. Denn es gelten zahlreiche Ausnahmen, die Regelung schließt viele Schmerzmittel aus. Das könnte dazu führen, dass identisch zusammengesetzte Produkte einmal mit und einmal ohne Warnhinweise vertrieben werden. Selbst wenn sie derselben Dachmarke angehören und nahezu identisch aussehen.
Die Analgetika-Warnhinweisverordnung (AnalgetikaWarnHV) gilt für Humanarzneimittel, die „ausschließlich zur Behandlung leichter bis mäßig starker Schmerzen oder von Fieber“ zugelassen sind. Für diese Präparate ist ein entsprechender Hinweis künftig Pflicht. Eingeschlossen sind Arzneimittel zur oralen oder rektalen Applikation, die nicht der Verschreibungspflicht unterliegen und Acetylsalicylsäure, Diclofenac, Ibuprofen, Naproxen, Paracetamol, Phenazon oder Propyphenazon enthalten.
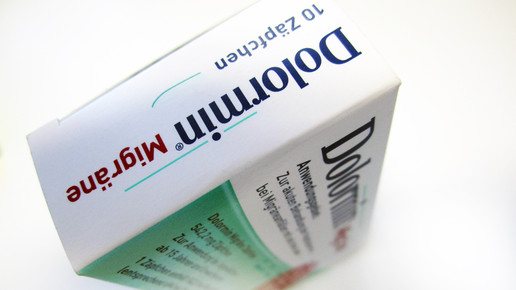
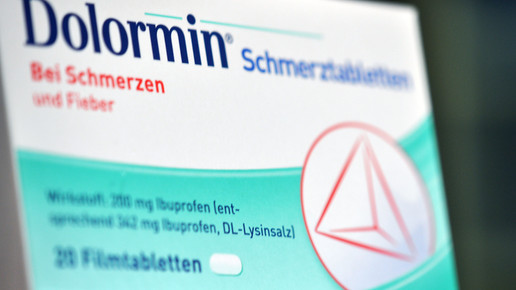
Je nachdem, wie die Indikation lautet, sind selbst identisch zusammengesetzt Präparate betroffen oder nicht. Bei großen Marken wie Dolormin, Thomapyrin oder Aspirin gibt es zahlreiche Varianten, die bei unterschiedlichen Beschwerdebildern eingesetzt werden. Aspirin Migräne unterscheidet sich in der Zusammensetzung vom Klassiker nicht, muss aber wegen der Indikation im Beipackzettel nicht mit einem Warnhinweis versehen werden. Dasselbe gilt für Dolormin – auch hier müssen die Varianten gegen Migräne sowie gegen Regelschmerzen nicht deklariert werden, die identisch zusammengesetzten Schwesterprodukte Dolormin extra und Dolormin GS dagegen schon. Thomapyrin intensiv ist ebenfalls ausgenommen, Thomapyrin classic nicht.
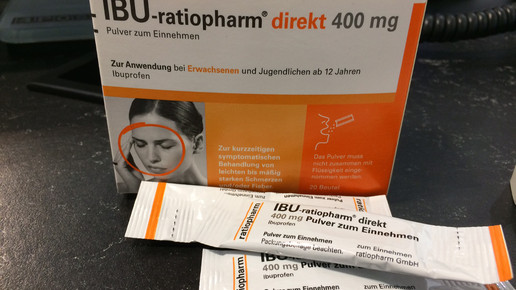
Noch verwirrender ist es bei Ibuprofen Ratiopharm: Das Direktgranulat bekommt einen Hinweis, die Tabletten mit Lysinat dagegen wegen einer zusätzlichen Indikation „Migräne“ nicht. Damit ist das Generikum auch im Vergleich zu den Markenprodukten wie Dolormin extra im Vorteil, die identisch zusammengesetzt sind, aber den Warnhinweis tragen müssen. Bei Phenazon greift die Neuregelung komplett ins Leere: Die beiden einzigen OTC-Präparate auf dem Markt ist Migräne Kranit (Krewel Meuselbach) und Eumed (Strathmann), die bei Migräne eingesetzt werden und daher nicht betroffen sind.
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) bestätigt: „Kombinationsarzneimittel, die einen der in der § 1 AnalgetikaWarnHV genannten Wirkstoffe enthalten, können in den Anwendungsbereich der Verordnung fallen. Die Anwendung der Verordnung hängt aber von mehreren Faktoren, die kumulativ erfüllt sein müssen, ab“, teilt eine Sprecherin mit. „Neben den enthaltenen Wirkstoffen ist unter anderem auch das zugelassene Anwendungsgebiet entscheidend: Ausschließlich zur Behandlung leichter bis mäßig starker Schmerzen oder von Fieber vorgesehene Arzneimittel müssen den Warnhinweis tragen.“
Laut BfArM sind auch Kombinationsarzneimittel zur symptomatischen Behandlung grippaler Infekte wie beispielsweise Boxagrippal (Ibuprofen/Pseudoephedrin, Sanofi) und Wick Daymed Erkältungskapseln (Paracetamol/Phenylpropanol/Dextromethorphan, P&G) nicht betroffen. Denn die Arzneimittel „sind für weitere Indikationen zugelassen und deshalb nicht vom Anwendungsbereich der Verordnung umfasst“.
Betroffen sind auch Arzneimittel nach § 1 a Absatz 8 und 9 der Apothekenbetriebsordnung (ApBetrO), sprich Rezeptur- und Defekturarzneimittel. Die AnalgetikaWarnHV gilt für rein nationale Zulassungen sowie jene aus dem gegenseitigen Anerkennungsverfahren oder dem dezentralen Verfahren sowie Parallelimport- und Standardzulassungen. Arzneimittel, die entsprechend den rechtlichen Vorgaben als Prüfpräparate eingestuft werden, sind nicht betroffen.
Die Geschichte der Analgetika-WarnHV reicht nunmehr zehn Jahre zurück. Seit etwa 2008 wurde über den Hinweis diskutiert. Ursprünglich sollten gar alle OTC-Analgetika der Verschreibungspflicht unterstellt werden, getroffen hat es schließlich nur Paracetamol in Großpackungen. Zahlreiche Vorschläge wurden abgelehnt und schließlich einigte man sich auf den jetzt eingeführten Hinweis: „Bei Schmerzen oder Fieber ohne ärztlichen Rat nicht länger anwenden als in der Packungsbeilage vorgegeben.“ Eine optimale und zeitgemäße Lösung ist der Hinweis zwar nicht, aber immerhin konnten sich die Beteiligten auf einen Vorschlag einigen. Etwa zehn Millionen Packungen pro Jahr sind betroffen und in spätestens fünf Jahren ist die Diskussion Geschichte.
Arzneimittel, die vor dem 1. Juli zugelassen wurden, müssen mit einer Übergangsfrist von zwei Jahren – bis zum 30. Juni 2020 – den Warnhinweis in deutlich lesbarer Schrift und dauerhaft auf der Vorderseite der Verpackung tragen. Alle OTC-Analgetika, die nach dem 1. Juli zugelassen werden, dürfen ab sofort mit dem Warnhinweis in den Verkehr gebracht werden. Ursprünglich wollte man den Herstellern nur eine Übergangsfrist von drei Monaten gewähren.
Apotheken müssen laut Heilmittelwerbegesetz (HWG) den Warnhinweis bei der Erstellung von Werbeflyern berücksichtigen, ein fehlen kann zur Abmahnfalle werden. In § 4 heißt es: „Jede Werbung für Arzneimittel im Sinne des § 2 Absatz 1 oder Absatz 2 Nummer 1 des Arzneimittelgesetzes (AMG) muss folgende Angaben enthalten: […] Nummer 7: Warnhinweise, soweit sie für die Kennzeichnung der Behältnisse und äußeren Umhüllungen vorgeschrieben sind.“ Jedoch nicht bei den erwähnten Grippemitteln.








































APOTHEKE ADHOC Debatte