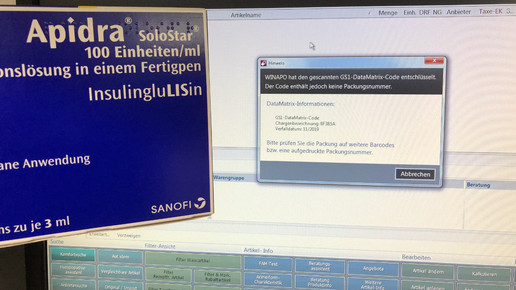
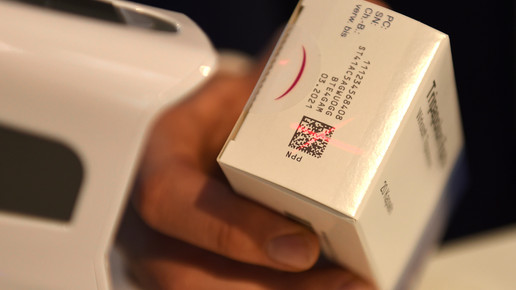
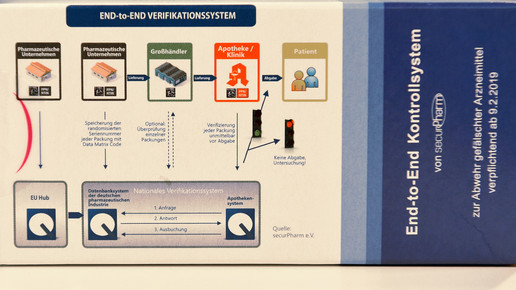
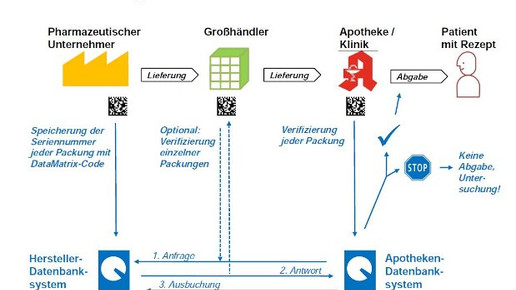
Am 9. Februar 2019 wird Securpharm scharf gestellt. Die Vorbereitungen laufen auf Hochtouren. Dennoch ist nicht ausgeschlossen, dass das System zur Verbesserung der Arzneimittelsicherheit nicht von Anbeginn reibungslos läuft. Bundesgesundheitsminister Jens Spahn (CDU) will Verstöße von Herstellern, Großhändlern und Apothekern gegen die neuen Regeln mit Bußgeldern ahnden. Das sieht eine Ergänzung im Gesetz für mehr Sicherheit in der Arzneimittelversorgung (GSAV) vor.
Die bisherigen Securpharm-Regeln sehen keine Sanktionen vor. Die Androhung von Bußgeldern sei erforderlich „zur Durchsetzung der Pflichten“ aus der Delegierten-Verordnung, heißt es im Gesetzentwurf. Für Hersteller gilt eine unverzügliche Meldepflicht, wenn Grund zur Annahme besteht, dass die Verpackung des Arzneimittels manipuliert wurde oder die Überprüfung der Sicherheitsmerkmale ergibt, dass das Arzneimittel nicht echt sein könnte. Erfolgt keine sofortige Meldung, könnten dann Bußgelder verhängt werden. Das GSAV soll zum 1. Juli 2019 in Kraft treten.
Bußgelder können auch gegen Großhändler und Apotheker verhängt werden. In § 97 Arzneimittelgesetz (AMG) heißt es dazu künftig nach dem Referentenentwurf des BMG: „Ordnungswidrig handelt, wer gegen die Delegierte Verordnung (EU) 2016/161 verstößt, indem er vorsätzlich oder fahrlässig entgegen Artikel 24 ein Arzneimittel abgibt oder es ausführt oder die zuständigen Behörden nicht oder nicht rechtzeitig informiert, entgegen Artikel 30 ein Arzneimittel an die Öffentlichkeit abgibt oder die zuständigen Behörden nicht oder nicht rechtzeitig informiert, oder entgegen Artikel 37d nicht für Warnung der zuständigen Behörden, der Europäischen Arzneimittel-Agentur oder der Europäische Kommission sorgt.“
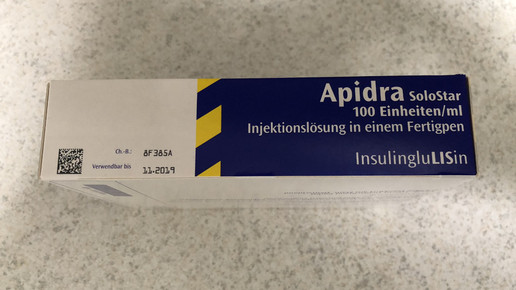
Das GSAV enthält aber auch eine Erleichterung für Hersteller bei der zulässigen Beschriftung der Arzneimittelpackungen: Das Ablaufdatum muss nicht mehr mit den ausgeschriebenen Worten „verwendbar bis“ gekennzeichnet werden, sondern kann auch mit der Beschriftung „verw. bis“ abgekürzt werden.
Entschieden wird im GSAV auch der sogenannte „Pflasterstreit“ zwischen Spahn und Josef Hecken: Der Vorsitzende des Gemeinsamen Bundesausschusses (G-BA) hatte das BMG wegen eines Streits um die Abgrenzung von Verbandmitteln und sonstigen Produkten zur Wundbehandlung verklagt. Der G-BA hatte aus Sicht des BMG eine zu enge Definition gezogen. Das hatte das Ministerium beanstandet. Aber Hecken wollte nicht klein bei geben. Jetzt stellt das BMG die Rechtslage aus seiner Sicht klar: „Die Eigenschaft als Verbandmittel entfällt insbesondere nicht, wenn ein Gegenstand ergänzend weitere Wirkungen im Verbandmittel oder in der Wunde entfaltet, die der Wundheilung dienen, beispielsweise, indem er eine Wunde feucht hält, reinigt, geruchsbindend oder antimikrobiell wirkt“, heißt es im Gesetzentwurf.
Der G-BA hatte die Auffassung vertreten, dass es für die Bestimmung der Hauptwirkung als Verbandmittel nicht belanglos ist, „ob und welche konkreten Wirkungen ein Produkt neben dem Bedecken und/oder Aufsaugen entfaltet, um es als ‚sonstiges Produkt zur Wundbehandlung‘ einer Bewertung des Nutzens für die Patienten unterziehen zu könne“.
Kassenpatienten haben laut Leistungskatalog Anspruch auf die Versorgung mit Verbandmitteln. Mit dem neuen Gesetz zur Stärkung der Heil- und Hilfsmittelversorgung (HHVG) hatte der Gesetzgeber den Anspruch durch eine Definition des Begriffes konkretisiert. Der G-BA wurde vom Gesetzgeber beauftragt, bis zum 30. April 2018 Näheres zur Abgrenzung dieser Verbandmittel von „sonstigen Produkten der Wundbehandlung“ zu regeln. Letztere sind keine Verbandmittel und deswegen nicht von vornherein durch die Ärzte verordnungsfähig. Sie sind nur dann eine GKV-Leistung, wenn sie vom G-BA als medizinisch notwendig eingestuft werden.
Zur Förderung der Verordnung und Abgabe von Biosimilars werden Regelungen zur Austauschbarkeit und zur Festlegung von Wirtschaftlichkeitszielen in den Arznei- und Heilmittelvereinbarungen geschaffen. Der G-BA wird verpflichtet, in seinen Richtlinien unverzüglich Hinweise zur Austauschbarkeit von Biosimilars sowie wirkstoffgleichen biologischen Arzneimitteln festzulegen.
Im Betäubungsmittelgesetz wird eine Möglichkeit geschaffen, neue psychoaktive Stoffe (NPS), für die auf EU-Ebene auf der Grundlage einer Risikobewertung festgestellt wurde, dass sie ein hohes Risiko für die öffentliche Gesundheit darstellen und die deshalb in die Definition von Drogen aufgenommen wurden, in einem vereinfachten und damit beschleunigten Verfahren in die Anlagen des BtMG aufzunehmen.
Die Arzneimittelbehörden von Bund und Ländern müssen Erklärungen ihrer Mitarbeiter und Berater zu möglichen Interessenkonflikten im Zusammenhang mit der pharmazeutischen Industrie veröffentlichen. „Die Veröffentlichung dient der Sicherung der Lauterkeit der behördlichen Entscheidung sowie der Stärkung der Transparenz im behördlichen Entscheidungsprozess“, heißt es dazu.
Die erlaubnisfreie Herstellung von Arzneimitteln zur persönlichen Anwendung bei einem Patienten durch eine Person, die nicht Arzt ist, wird auf auf nicht verschreibungspflichtige Arzneimittel beschränkt. Hintergrund sind Behandlungen durch Heilpraktiker. Auch die Frischzellenbehandlung wird eingeschränkt.
Bei Standardzulassungen wird die Verpflichtung zur Anhörung von Sachverständigen gestrichen, da es sich in der Folge nur noch um technische Anpassungen bei den bestehenden Monographien handelt. Bei Anwendungsbeobachtungen müssen die Betriebsstättennummer und die Praxisadresse gemeldet werden. Für nicht zulassungs- oder genehmigungspflichtige Arzneimittel für neuartige Therapien wir eine Dokumentations- und Meldepflicht eingeführt: Der Arzt muss alle Nebenwirkungen, die etwa im Zusammenhang mit einer Gentherapie auftreten, erfassen und die Unterlagen zu schwerwiegenden Fällen unverzüglich, spätestens aber innerhalb von 15 Tagen nach Bekanntwerden, der zuständigen Behörde elektronisch anzeigen.
4-Anilino-N-phenethylpiperidin (ANPP) und N-Phenethyl-4-piperidon (NPP) werden als Stoffe in Kategorie 1 nach Grundstoffüberwachungsgesetz (GÜG) aufgenommen, da sie Ausgangsstoffe für die Herstellung von Fentanyl und Analoga sind.
Auch die Finanzierung der Ausbildung im Bereich Pflege wird mit dem Gesetz geregelt. Berufsanfänger im ersten Ausbildungsjahr entlasten die voll ausgebildeten Pflegefachkräfte in der Regel in einem geringeren Umfang als Auszubildende im zweiten oder dritten Jahr der Ausbildung. Aus diesem Grund wird die Anrechnung von Auszubildenden auf voll ausgebildete Pflegefachkräfte für das erste Ausbildungsjahr ausgeschlossen. Damit werden die Ausbildungsvergütungen im ersten Ausbildungsjahr vollständig refinanziert.














































APOTHEKE ADHOC Debatte